题目内容
(2012?百色二模)X、Y、Z为短周期元素,X原子的最外层电子数是Y原子最外层电子数的2倍,但Y的原子序数比X的原子序数多5,Z原子的最外层电子数比Y多3.下列叙述正确的是( )
分析:X、Y、Z为短周期元素,X原子的最外层电子数是Y 原子最外层电子数的2倍,但Y的原子序数比X的原子序数多5,则X、Y不可能处于同一周期,若X处于第一周期,则X只能为He,Y最外层电子数为1,为Li或Na,不满足原子序数相差5,故X不能处于第一周期,则X处于第二周期、Y处于第三周期,
令Y的最外层电子数为a,则X的最外层电子数为2a,根据原子序数之差可得,2+8+a-(2+2a)=5,解得a=3,则X为氧元素、Y为Al元素;Z原子的最外层电子数比Y多3,则Z原子最外层电子数为6,则Z只能为硫元素,据此解答.
令Y的最外层电子数为a,则X的最外层电子数为2a,根据原子序数之差可得,2+8+a-(2+2a)=5,解得a=3,则X为氧元素、Y为Al元素;Z原子的最外层电子数比Y多3,则Z原子最外层电子数为6,则Z只能为硫元素,据此解答.
解答:解:X、Y、Z为短周期元素,X原子的最外层电子数是Y 原子最外层电子数的2倍,但Y的原子序数比X的原子序数多5,则X、Y不可能处于同一周期,若X处于第一周期,则X只能为He,Y最外层电子数为1,为Li或Na,不满足原子序数相差5,故X不能处于第一周期,则X处于第二周期、Y处于第三周期,
令Y的最外层电子数为a,则X的最外层电子数为2a,根据原子序数之差可得,2+8+a-(2+2a)=5,解得a=3,则X为氧元素、Y为Al元素;Z原子的最外层电子数比Y多3,则Z原子最外层电子数为6,则Z只能为硫元素,
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Al>S>O,故A错误;
B.X为氧元素,其单质有O2、O3,存在同素异形体,故B错误;
C.H2S水溶液在空气中易被氧气氧化,容易变质,故C错误;
D.X和Y元素形成的化合物为Al2O3,Z的最高价氧化物的水化物为硫酸,氧化铝与硫酸反应生成硫酸铝,故D正确;
故选:D.
令Y的最外层电子数为a,则X的最外层电子数为2a,根据原子序数之差可得,2+8+a-(2+2a)=5,解得a=3,则X为氧元素、Y为Al元素;Z原子的最外层电子数比Y多3,则Z原子最外层电子数为6,则Z只能为硫元素,
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Al>S>O,故A错误;
B.X为氧元素,其单质有O2、O3,存在同素异形体,故B错误;
C.H2S水溶液在空气中易被氧气氧化,容易变质,故C错误;
D.X和Y元素形成的化合物为Al2O3,Z的最高价氧化物的水化物为硫酸,氧化铝与硫酸反应生成硫酸铝,故D正确;
故选:D.
点评:本题考查结构性质位置关系,推断元素是关键,侧重对学生的逻辑推理能力考查,难度中等,注意基础知识的掌握.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
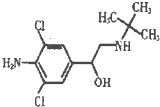 (2012?百色二模)瘦肉精学名盐酸克伦特罗,其结构简式如图.下列关于瘦肉精的说法不正确的是
(2012?百色二模)瘦肉精学名盐酸克伦特罗,其结构简式如图.下列关于瘦肉精的说法不正确的是