题目内容
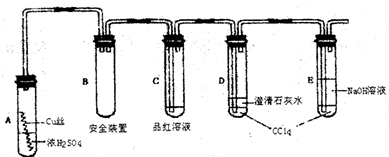
某研究性学习小组为了研究Cu与浓H2SO4的反应和比较Cu的+1价化合物与+2价化合物的稳定性,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出)实验选用细铜丝、98.3%H2SO4、品红溶液、澄清石灰水、CCl4、NaOH溶液等药品,铜丝被卷成螺旋状,一端投入浓H2SO4中,另一端露置在液面上方.
以下是该学习小组部分交流记录及后续探究实验的记录.
材料一:小组交流记录
学生1:加热前,无现象发生;加热后,液面下铜丝变黑,产生气泡,有细小黑色颗粒状物质从铜丝表面进入浓硫酸中,黑色物质是什么?值得探究!
学生2:我也观察到黑色颗粒状物质,后来逐渐转变为灰白色固体,我想该灰白色固体极有可能是未溶于浓硫酸的CuSO4.
学生3:你们是否注意到液面以上的铜丝也发黑,而且试管上部内壁有少量淡黄色S固体凝聚,会不会液面以上的铜丝与硫发生了反应,我查资料发现:2Cu+S
Cu2S(黑色)
材料二、探究实验剪辑
实验1:将光亮的铜丝在酒精灯火焰上灼烧变黑,然后插入稀硫酸中,铜丝重新变得光亮,溶液呈蓝绿色;将光亮的铜丝置入加热的硫蒸气中变黑,然后插入稀硫酸中无变化.
实验2:截取浓硫酸液面上方变黑的铜丝,插入稀硫酸中无变化;将浓硫酸液面下方变黑的铜丝,插入稀硫酸、黑色明显变浅,溶液呈蓝绿色.
实验3:将溶液中的黑色颗粒状物质,经过滤、稀硫酸洗、蒸馏水洗、干燥后放入氧气流中加热,然后冷却,用电子天平称重发现质量减小10%左右.
根据上述材料回答下列问题:
(1)A试管上方的长导管的作用是;
的作用是
(2)加热过程中,观察到A试管中出现大量白色烟雾,起初部分烟雾在试管上部内壁析出淡黄色固体物质,在持续加热浓硫酸(沸腾)时,淡黄色固体物质又慢慢地消失.写出淡黄色固体消失的化学反应方程式:
(3)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,但始终未见D试管中澄清石灰水出现浑浊或沉淀.学生1猜想是由于SO2溶解度较大,生成了Ca(SHO3)2的缘故.请你设计实验验证学生1的猜想
(4)根据上述研究,结合所学知识,你认为液面下方铜丝表面的黑色物质成分是:
(5)学生2将反应后的反应液稀释后进行检验,发现溶液呈酸性,对比,学生2提出猜想是:铜与浓硫酸反应生成的硫酸铜水解使溶液呈酸性,请写出该水解反应的离子方程式:
你的猜想是:
请你设计一个简单的实验以验证你的猜想:
(6)该研究性学习小组的同学为了比较Cu的+1价化合物和+2价化合物的稳定性,他们取98gCu(OH)2固体,加热至80℃-100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末X.冷却后称量,X的质量为72g.向X中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在,据此可推得,X的化学式为

以下是该学习小组部分交流记录及后续探究实验的记录.
材料一:小组交流记录
学生1:加热前,无现象发生;加热后,液面下铜丝变黑,产生气泡,有细小黑色颗粒状物质从铜丝表面进入浓硫酸中,黑色物质是什么?值得探究!
学生2:我也观察到黑色颗粒状物质,后来逐渐转变为灰白色固体,我想该灰白色固体极有可能是未溶于浓硫酸的CuSO4.
学生3:你们是否注意到液面以上的铜丝也发黑,而且试管上部内壁有少量淡黄色S固体凝聚,会不会液面以上的铜丝与硫发生了反应,我查资料发现:2Cu+S
| ||
材料二、探究实验剪辑
实验1:将光亮的铜丝在酒精灯火焰上灼烧变黑,然后插入稀硫酸中,铜丝重新变得光亮,溶液呈蓝绿色;将光亮的铜丝置入加热的硫蒸气中变黑,然后插入稀硫酸中无变化.
实验2:截取浓硫酸液面上方变黑的铜丝,插入稀硫酸中无变化;将浓硫酸液面下方变黑的铜丝,插入稀硫酸、黑色明显变浅,溶液呈蓝绿色.
实验3:将溶液中的黑色颗粒状物质,经过滤、稀硫酸洗、蒸馏水洗、干燥后放入氧气流中加热,然后冷却,用电子天平称重发现质量减小10%左右.
根据上述材料回答下列问题:
(1)A试管上方的长导管的作用是;
导气、冷凝、回流
导气、冷凝、回流
;D、E两支试管中CCl4的作用是
防止倒吸
防止倒吸
.(2)加热过程中,观察到A试管中出现大量白色烟雾,起初部分烟雾在试管上部内壁析出淡黄色固体物质,在持续加热浓硫酸(沸腾)时,淡黄色固体物质又慢慢地消失.写出淡黄色固体消失的化学反应方程式:
S+2H2SO4(浓)
3SO2↑+2H2O
| ||
S+2H2SO4(浓)
3SO2↑+2H2O
.
| ||
(3)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,但始终未见D试管中澄清石灰水出现浑浊或沉淀.学生1猜想是由于SO2溶解度较大,生成了Ca(SHO3)2的缘故.请你设计实验验证学生1的猜想
取样后,向其中加氢氧化钠溶液,观察是否有沉淀生成(其他答案也合理)
取样后,向其中加氢氧化钠溶液,观察是否有沉淀生成(其他答案也合理)
.(4)根据上述研究,结合所学知识,你认为液面下方铜丝表面的黑色物质成分是:
CuO、CuS、Cu2S
CuO、CuS、Cu2S
.(写化学式)(5)学生2将反应后的反应液稀释后进行检验,发现溶液呈酸性,对比,学生2提出猜想是:铜与浓硫酸反应生成的硫酸铜水解使溶液呈酸性,请写出该水解反应的离子方程式:
Cu2++H2O Cu(OH)2+2H+
Cu(OH)2+2H+
 Cu(OH)2+2H+
Cu(OH)2+2H+Cu2++H2O Cu(OH)2+2H+
Cu(OH)2+2H+
. Cu(OH)2+2H+
Cu(OH)2+2H+你的猜想是:
铜和浓硫酸反应的实验中硫酸过量使溶液显酸性
铜和浓硫酸反应的实验中硫酸过量使溶液显酸性
;请你设计一个简单的实验以验证你的猜想:
取稀释后的溶液适量于试管中,加入足量的铁粉,若有无色无味的气体产生,证明硫酸过量(其他答案也合理)
取稀释后的溶液适量于试管中,加入足量的铁粉,若有无色无味的气体产生,证明硫酸过量(其他答案也合理)
.(6)该研究性学习小组的同学为了比较Cu的+1价化合物和+2价化合物的稳定性,他们取98gCu(OH)2固体,加热至80℃-100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末X.冷却后称量,X的质量为72g.向X中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在,据此可推得,X的化学式为
Cu2O
Cu2O
,可以得出的结论是 高于100°C时Cu2O比CuO稳定,在溶液中Cu2+比Cu+稳定
高于100°C时Cu2O比CuO稳定,在溶液中Cu2+比Cu+稳定
.分析:(1)长导管除了导气作用之外,还可以让气体冷凝,回流;二氧化硫和强碱的反应十分剧烈,要注意防止倒吸现象的发生;
(2)硫在加热时能和浓硫酸反应;
(3)酸式盐和强碱中的氢氧根反应能得到正盐;
(4)含有铜元素的常见黑色物质有CuO、CuS、Cu2S,结合实际来回答;
(5)铜离子是弱碱阳离子,有弱就水解,水解显酸性,根据实验实际情况来判断溶液显酸性的可能原因并进行试验验证;
(6)根据质量关系结合原子守恒来判断物质的组成情况,根据物质转化的条件和存在的状态来判断其稳定性.
(2)硫在加热时能和浓硫酸反应;
(3)酸式盐和强碱中的氢氧根反应能得到正盐;
(4)含有铜元素的常见黑色物质有CuO、CuS、Cu2S,结合实际来回答;
(5)铜离子是弱碱阳离子,有弱就水解,水解显酸性,根据实验实际情况来判断溶液显酸性的可能原因并进行试验验证;
(6)根据质量关系结合原子守恒来判断物质的组成情况,根据物质转化的条件和存在的状态来判断其稳定性.
解答:解:(1)根据实验装置,长导管的作用一定是能导气,但气体在导管中时间一长就会冷凝,回流,二氧化硫和强碱的反应十分剧烈,可以采用四氯化碳的作用来达到防止倒吸现象的发生的目的,
故答案为:导气、冷凝、回流;防止倒吸;
(2)浓硫酸具有强氧化性,硫在加热时能和浓硫酸反应,
故答案为:S+2H2SO4(浓)
3SO2↑+2H2O;
(3)Ca(HSO3)2能和强碱反应生成溶解度较小的亚硫酸钙,故答案为:取样后,向其中加氢氧化钠溶液,观察是否有沉淀生成;
(4)将浓硫酸液面下方变黑的铜丝,插入稀硫酸、黑色明显变浅,溶液呈蓝绿色,说明黑色物质部分溶于稀硫酸,
故答案为:CuO、CuS、Cu2S;
(5)铜离子是弱碱阳离子,有弱就水解,水解显酸性,方程式为:Cu2++H2O Cu(OH)2+2H+;溶液显酸性的可能原因是硫酸过量,可以加入金属铁来检验溶液中氢离子的存在,
Cu(OH)2+2H+;溶液显酸性的可能原因是硫酸过量,可以加入金属铁来检验溶液中氢离子的存在,
故答案为:Cu2++H2O Cu(OH)2+2H+;铜和浓硫酸反应的实验中硫酸过量使溶液显酸性;取稀释后的溶液适量于试管中,加入足量的铁粉,若有无色无味的气体产生,证明硫酸过量(其他答案也合理);
Cu(OH)2+2H+;铜和浓硫酸反应的实验中硫酸过量使溶液显酸性;取稀释后的溶液适量于试管中,加入足量的铁粉,若有无色无味的气体产生,证明硫酸过量(其他答案也合理);
(6)98gCu(OH)2固体加热至80℃-100℃时,得到黑色固体粉末为氧化铜80g,加热到1000℃以上,黑色粉末氧化铜全部变成红色粉末其质量为72g,根据2CuO~Cu2O知,X恰好为Cu2O,根据题目信息:Cu(OH)2固体加热至80℃-100℃时,得到黑色固体粉末为氧化铜,加热到1000℃以上,得到的是氧化亚铜,可知高于100°C时Cu2O比CuO稳定,将黑的铜丝,插入稀硫酸、黑色明显变浅,溶液呈蓝绿色,说明在溶液中Cu2+比Cu+稳定,
故答案为:Cu2O;高于100°C时Cu2O比CuO稳定,在溶液中Cu2+比Cu+稳定.
故答案为:导气、冷凝、回流;防止倒吸;
(2)浓硫酸具有强氧化性,硫在加热时能和浓硫酸反应,
故答案为:S+2H2SO4(浓)
| ||
(3)Ca(HSO3)2能和强碱反应生成溶解度较小的亚硫酸钙,故答案为:取样后,向其中加氢氧化钠溶液,观察是否有沉淀生成;
(4)将浓硫酸液面下方变黑的铜丝,插入稀硫酸、黑色明显变浅,溶液呈蓝绿色,说明黑色物质部分溶于稀硫酸,
故答案为:CuO、CuS、Cu2S;
(5)铜离子是弱碱阳离子,有弱就水解,水解显酸性,方程式为:Cu2++H2O
 Cu(OH)2+2H+;溶液显酸性的可能原因是硫酸过量,可以加入金属铁来检验溶液中氢离子的存在,
Cu(OH)2+2H+;溶液显酸性的可能原因是硫酸过量,可以加入金属铁来检验溶液中氢离子的存在,故答案为:Cu2++H2O
 Cu(OH)2+2H+;铜和浓硫酸反应的实验中硫酸过量使溶液显酸性;取稀释后的溶液适量于试管中,加入足量的铁粉,若有无色无味的气体产生,证明硫酸过量(其他答案也合理);
Cu(OH)2+2H+;铜和浓硫酸反应的实验中硫酸过量使溶液显酸性;取稀释后的溶液适量于试管中,加入足量的铁粉,若有无色无味的气体产生,证明硫酸过量(其他答案也合理);(6)98gCu(OH)2固体加热至80℃-100℃时,得到黑色固体粉末为氧化铜80g,加热到1000℃以上,黑色粉末氧化铜全部变成红色粉末其质量为72g,根据2CuO~Cu2O知,X恰好为Cu2O,根据题目信息:Cu(OH)2固体加热至80℃-100℃时,得到黑色固体粉末为氧化铜,加热到1000℃以上,得到的是氧化亚铜,可知高于100°C时Cu2O比CuO稳定,将黑的铜丝,插入稀硫酸、黑色明显变浅,溶液呈蓝绿色,说明在溶液中Cu2+比Cu+稳定,
故答案为:Cu2O;高于100°C时Cu2O比CuO稳定,在溶液中Cu2+比Cu+稳定.
点评:本题是有关铜及其化合物之间的转化知识的综合题目,考查角度广,难度很大.

练习册系列答案
相关题目
某研究性学习小组为了探索镁粉与FeCl3溶液的反应机理,做了如下两组实验:
①将镁粉投入冷水中,未见明显现象;
②将镁粉投入FeCl3溶液中,观察到有气泡产生,溶液颜色逐渐变浅,同时逐渐产生红褐色沉淀.
则下列有关镁与FeCl3溶液反应的叙述中,正确的是( )
①将镁粉投入冷水中,未见明显现象;
②将镁粉投入FeCl3溶液中,观察到有气泡产生,溶液颜色逐渐变浅,同时逐渐产生红褐色沉淀.
则下列有关镁与FeCl3溶液反应的叙述中,正确的是( )
| A、镁只与FeCl3溶液中的Fe3+直接反应 | B、气泡是镁与FeCl3溶液中的水直接反应产生的 | C、红褐色沉淀是镁与水反应生成的Mg(OH)2与Fe3+反应所得 | D、汽泡是镁与FeCl3水解生成的盐酸反应产生的 |
 “白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一.镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标.某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一.镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标.某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案: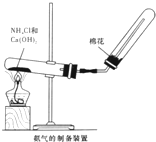 某研究性学习小组为了制取氨气和探究氨气的有关性质,进行了下列实验.
某研究性学习小组为了制取氨气和探究氨气的有关性质,进行了下列实验.