题目内容
【题目】在容积固定的2L密闭容器中,一定条件下发生如下反应:X(g)+2Y(g)nZ(g),反应过程中各物质的量与时间的关系如图所示.完成下列填空:
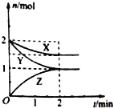
(1)n=______;
(2)Y的平衡浓度为_______;
(3)反应开始至平衡,X 的反应速率v(X)=______.
【答案】2 0.5mol·L-1 0.125mol·L-1·min-1
【解析】
根据图像可知,反应起始时反应物X、Y的起始量均为2mol,平衡时,X、Y、Z的平衡量分别为1.5mol、1mol、1mol,则变化量分别是0.5mol、1mol、1mol。
(1)由图可知,平衡时△n(Y)=2mol-1mol=1mol,△n(Z)=1mol,则1:1=2:n,故n=2,故答案为:2;
(2)平衡时Y为1mol,Y的平衡浓度为0.5mol/L,故答案为:0.5mol/L;
(3)由方程式可知△n(X)=![]() △n(Y)=0.5mol,则v(X)=
△n(Y)=0.5mol,则v(X)=![]() =0.125 mol·L-1·min-1,故答案为:0.125mol·L-1·min-1。
=0.125 mol·L-1·min-1,故答案为:0.125mol·L-1·min-1。

【题目】乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇的一种反应原理为: 2CO(g)+4H2 (g) ![]() CH3CH2OH(g)+H2O(g) △H= — 256.1 kJ·mol—1。
CH3CH2OH(g)+H2O(g) △H= — 256.1 kJ·mol—1。
CO(g)+H2O(g)![]() CO2(g)+H2(g) △H= — 41.2 kJ·mol—1
CO2(g)+H2(g) △H= — 41.2 kJ·mol—1
已知:H2O(l)=H2O(g) △H= + 44 kJ·mol—1
(1)以CO2(g)与H2(g)为原料也可合成乙醇,其热化学方程式如下:2CO2(g)+6H2(g) ![]() CH3CH2OH(g)+3H2O(l) △H=___________。
CH3CH2OH(g)+3H2O(l) △H=___________。
(2)CH4和H2O(g)在催化剂表面发生反应CH4+H2O![]() CO+3H2,该反应在不同温度下的化学平衡常数如下表:
CO+3H2,该反应在不同温度下的化学平衡常数如下表:
温度/℃ | 800 | 1000 | 1200 | 1400 |
平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
①该反应是__________反应(填“吸热”或“放热”);
②T℃时,向1L密闭容器中投入1molCH4和1mol H2O(g), 平衡时c(CH4)=0.5mol·L—1,该温度下反应CH4+H2O![]() CO+3H2的平衡常数K=_____________。
CO+3H2的平衡常数K=_____________。
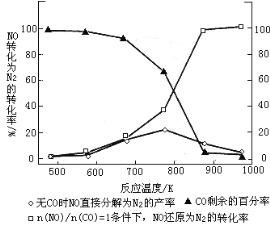
(3)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag-ZSM-5 为催化剂,测得NO转化为N2的转化率随温度变化情况如下图
①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为___________;在n(NO)/n(CO)=1的条件下,应控制的最佳温度在_____左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染。写出CH4与NO2发生反应的化学方程式:_____________。
(4)乙醇-空气燃料电池中使用的电解质是搀杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子。该电池负极的电极反应式为________________________。

