题目内容
【题目】已知某校回收的含银悬浊废水中含有AgCl、Ag(NH3)2NO3、AgNO3、CH3COONH4、NaCl等,设计从废水中回收硝酸银的具体流程如下:
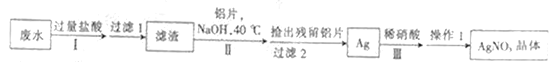
下列说法不正确的是
A. 步骤Ⅱ中发生的主要反应的离子方程:3AgCl+Al+4OH-=3Ag+AlO2-+3Cl-+2H2O
B. 实验中用铝粉代替铝片可以加快反应速率并简化实验操作
C. 步骤Ⅲ中若先将Ag氧化为Ag2O,再加入稀硝酸反应有利于环保
D. 操作Ⅰ包括蒸发浓缩、冷却结晶、过滤、洗涤等
【答案】B
【解析】
含银悬浊废水中含有AgCl、Ag(NH3)2NO3、AgNO3、CH3COONH4、NaCl等,加入盐酸后生成氯化银沉淀,过滤后,滤渣的主要成分是氯化银,在氯化银中加入铝片、氢氧化钠溶液后置换出银,然后用硝酸溶解得到硝酸银溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤得到硝酸银晶体,据此分析解答。
A、步骤Ⅱ中主要发生铝、氢氧化钠溶液与氯化银的置换反应,发生的主要反应的离子方程式为:3AgCl+Al+4OH-=3Ag+AlO2-+3Cl-+2H2O,故A正确;
B、若实验中用铝粉代替铝片可以加快反应速率,但置换出的银中混入了铝粉,还需要分离提纯,没有简化实验操作,故B错误;
C、银与稀硝酸反应会生成NO,污染环境,若先将Ag氧化为Ag2O,再加入稀硝酸反应,可以防止NO的生成,有利于环保,故C正确;
D、操作Ⅰ是从硝酸银溶液中获得硝酸银晶体,需要经过蒸发浓缩、冷却结晶、过滤、洗涤等,故D正确;
故选B。

练习册系列答案
相关题目