题目内容
20.下列试剂中可用于除去CO2中少量SO2杂质的有( )①饱和NaHCO3溶液 ②酸性KMnO4溶液 ③溴水 ④饱和Na2CO3溶液.
| A. | ②③④ | B. | ①③④ | C. | ①②③ | D. | ①②④ |
分析 CO2和SO2都为酸性气体,都可与强碱性溶液反应,SO2具有还原性,除去CO2中的SO2,可用强氧化性物质或饱和NaHCO3溶液,以此解答.
解答 解:①SO2可与饱和NaHCO3溶液反应生成CO2,但CO2不反应,可用于除杂,故正确;
②SO2可与酸性高锰酸钾反应,而二氧化碳不能,可除杂,故正确;
③SO2可与溴水反应,而二氧化碳不能,可除杂,故正确;
④二者均与碳酸钠反应,不能除杂,故错误;
故选C.
点评 本题考查物质的分离和提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,除杂时不能引入新的杂质,题目难度不大.

练习册系列答案
相关题目
10.苯环结构中不存在C-C单键与C=C双键的交替结构,可以作为证据的是( )
①苯不能使溴水褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤经测定,苯环上碳碳键的键长相等.
①苯不能使溴水褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤经测定,苯环上碳碳键的键长相等.
| A. | ①②④⑤ | B. | ①②③⑤ | C. | ①②③ | D. | ①② |
11.为了检验自来水中Cl一的存在,最好选用下列试剂中的( )
| A. | 石蕊试液 | B. | 四氯化碳 | ||
| C. | 硝酸银溶液和稀盐酸 | D. | 硝酸银溶液和稀硝酸 |
8.下列说法中正确的是( )
| A. | 标准状况下,11.2L N2和17g NH3中所含有的N原子数相同 | |
| B. | 9g H2O和0.5mol O2中含的原子数相同 | |
| C. | 20℃时,相同体积的N2、O2一定含有相同的分子数 | |
| D. | 在常温常压下,20mL CH4与60mL O2所含的原子个数比为1:3 |
15.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 滴入KSCN显红色的溶液:Na+、Cu2+、Br-、SO42- | |
| B. | 滴入酚酞显红色的溶液:Na+、Al3+、SO42-、Cl- | |
| C. | c(Fe2+)=1 mol•L-1的溶液:H+、Na+、Cl-、NO3- | |
| D. | 加入铝粉能产生大量H2的溶液:Na+、K+、Cl-、HCO3- |
5.已知A(g)+C(g)=D(g);△H=-Q1kJ/mol,B(g)+C(g)=E(g),△H=-Q2kJ/mol,Q1、Q2均大于0,且Q1>Q2,若A与B组成的混合气体1mol与足量的C反应,放热为Q3kJ,则原混合气体中A与B物质的量之比为( )
| A. | $\frac{{Q}_{3}-{Q}_{2}}{{Q}_{1}-{Q}_{3}}$ | B. | $\frac{{Q}_{1}-{Q}_{3}}{{Q}_{3}-{Q}_{2}}$ | C. | $\frac{{Q}_{3}-{Q}_{2}}{{Q}_{1}-{Q}_{2}}$ | D. | $\frac{{Q}_{1}-{Q}_{3}}{{Q}_{1}-{Q}_{2}}$ |
12.下列说法正确的是( )
| A. | 同物质的量的N2和HCl的原子数相同,分子数也相同 | |
| B. | 0.05mol H2SO4含有氧原子数的精确值为1.024×1023 | |
| C. | 0.1mol氯的微粒数约为6.02×1023个 | |
| D. | 1mol NaClO含有阿伏加德罗常数个氯分子 |
8.W粒子的结构如图所示,下列关于它的说法不正确的是( )
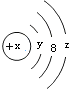

| A. | Y=2 | B. | 若X=14,它的氢化物的化学式为H2X | ||
| C. | 若X=18,则Z=8 | D. | 若X=17,它的氧化物化学式为W2O7 |
9.下列各组元素按第一电离能增加顺序排列的是( )
| A. | Na、Al、Mg | B. | Be、B、Li | C. | Li、Na、K | D. | O、F、N |