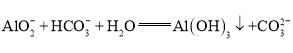题目内容
【题目】铅蓄电池是最常见的二次电池,电池总反应式为:Pb+PbO2+4H++2SO![]()
![]() 2PbSO4+2H2O,下列说法错误的是( )
2PbSO4+2H2O,下列说法错误的是( )
A.充电时,阴极反应式为:SO![]() +4H++PbO2+2e﹣═PbSO4+2H2O
+4H++PbO2+2e﹣═PbSO4+2H2O
B.充电时,两个电极的质量均减轻
C.电池放电时,电解质溶液的pH增大
D.电池放电时,负极可能会发生副反应:Pb+H2SO4═PbSO4+H2↑
【答案】A
【解析】
A.充电时,阴极电极反应式与原电池负极反应式相反,所以阴极反应式为PbSO4+2e-=Pb+SO42-,故A错误;
B.充电时,阴极电极反应式与原电池负极反应式相反,所以阴极反应式为PbSO4+2e-=Pb+SO42-,阳极电极反应式与原电池正极反应式相反,所以阳极反应式为PbSO4+2H2O-2e﹣═ SO![]() +4H++PbO2,电极质量均减轻,故B正确;
+4H++PbO2,电极质量均减轻,故B正确;
C.放电时,负极上Pb失电子发生氧化反应,电极反应式为Pb-2e-+SO42-=PbSO4,正极上二氧化铅得电子发生还原反应,电极反应式为SO![]() +4H++PbO2+2e﹣═PbSO4+2H2O,氢离子浓度减小了,所以电解质溶液的pH增大,故C正确;
+4H++PbO2+2e﹣═PbSO4+2H2O,氢离子浓度减小了,所以电解质溶液的pH增大,故C正确;
D.铅和稀硫酸能发生反应,负极可能会发生副反应:Pb+H2SO4=PbSO4+H2↑,故D正确;
故答案:A。

【题目】下列实验操作、现象、结论、因果关系均正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 向淀粉溶液中滴加稀硫酸,加热,再加碘水 | 溶液变蓝 | 淀粉没有水解 |
B | 将 |
| 有乙烯生成 |
C | 向 | 产生砖红色沉淀 | 葡萄糖具有还原性 |
D | 将乙醇加入浓硫酸中,快速加热到170℃,将产生的气体通入溴水 | 溴水褪色 | 不能证明有乙烯生成 |
A.AB.BC.CD.D