题目内容
【题目】下列实验操作、现象、结论、因果关系均正确的是( )
选项 | 实验操作 | 现象 | 结论 |
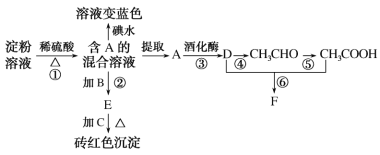
A | 向淀粉溶液中滴加稀硫酸,加热,再加碘水 | 溶液变蓝 | 淀粉没有水解 |
B | 将 |
| 有乙烯生成 |
C | 向 | 产生砖红色沉淀 | 葡萄糖具有还原性 |
D | 将乙醇加入浓硫酸中,快速加热到170℃,将产生的气体通入溴水 | 溴水褪色 | 不能证明有乙烯生成 |
A.AB.BC.CD.D
【答案】C
【解析】
A.向淀粉溶液中滴加稀硫酸,加热,再加碘水,观察到溶液变蓝,只能说明溶液还有淀粉,不能得出淀粉没有水解的结论,A不符合题意;
B. 将![]() 的乙醇溶液加入溴乙烷中加热,由于乙醇易挥发且乙醇可以使酸性高锰酸钾溶液褪色,故将产生的气体直接通入酸性
的乙醇溶液加入溴乙烷中加热,由于乙醇易挥发且乙醇可以使酸性高锰酸钾溶液褪色,故将产生的气体直接通入酸性![]() 溶液中,观察到
溶液中,观察到![]() 溶液褪色,不能得出有乙烯生成的结论,B不符合题意;
溶液褪色,不能得出有乙烯生成的结论,B不符合题意;
C.向![]()
![]()
![]() 溶液中滴入5滴
溶液中滴入5滴![]()
![]() 溶液,再加入
溶液,再加入![]()
![]() 的葡萄糖溶液混合加热,产生砖红色沉淀,葡萄糖具有还原性,该实验的实验操作、现象、结论、因果关系均正确,C符合题意;
的葡萄糖溶液混合加热,产生砖红色沉淀,葡萄糖具有还原性,该实验的实验操作、现象、结论、因果关系均正确,C符合题意;
D.将乙醇加入浓硫酸中,快速加热到170℃,在170℃温度以下乙醇和浓硫酸反应不可能得到SO2气体,故将产生的气体通入溴水,观察到溴水褪色,只能证明有乙烯生成,D不符合题意;
故答案为:C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
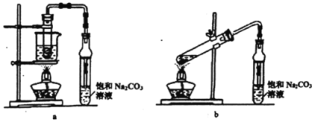
【题目】下列方案设计能达到实验目的的是
A | B | C | D |
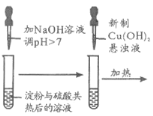
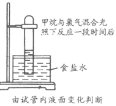
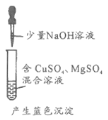
检验淀粉是否水解 | 由褪色快慢研究反应物浓度对反应速率的影响 | 证明发生了取代反应 | 验证Ksp[Cu(OH)2]<Ksp[Mg(OH)2 ] |
|
|
|
|
A.AB.BC.CD.D