题目内容
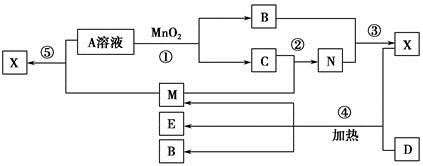
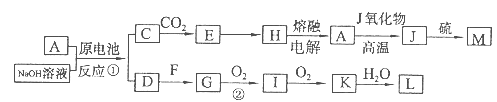
如图表示常见元素单质及化合物相应关系,某些生成物已略去。

已知:反应①为氯碱工业的基础反应;X、Y为常见金属,Z为形成酸雨的主要成分。请回答下列问题:
(1)D的电子式 ;H为 (填化学式)。
(2)完成下列方程式:
①空气中含量最高的气体与C反应的化学反应方程式 ;
②反应②的化学反应方程式 ;
③足量B通入H溶液的离子反应方程式 。

已知:反应①为氯碱工业的基础反应;X、Y为常见金属,Z为形成酸雨的主要成分。请回答下列问题:
(1)D的电子式 ;H为 (填化学式)。
(2)完成下列方程式:
①空气中含量最高的气体与C反应的化学反应方程式 ;
②反应②的化学反应方程式 ;
③足量B通入H溶液的离子反应方程式 。
(1)Na+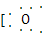 H]- NaHSO3
H]- NaHSO3
(2)①N2+3H2 2NH3
2NH3
②2Al+Fe2O3 2Fe+Al2O3(或2Al+3CuO
2Fe+Al2O3(或2Al+3CuO 3Cu+Al2O3)
3Cu+Al2O3)
③Cl2+HSO3-+H2O=2Cl-+SO42-+3H+
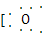 H]- NaHSO3
H]- NaHSO3(2)①N2+3H2
 2NH3
2NH3②2Al+Fe2O3
 2Fe+Al2O3(或2Al+3CuO
2Fe+Al2O3(或2Al+3CuO 3Cu+Al2O3)
3Cu+Al2O3)③Cl2+HSO3-+H2O=2Cl-+SO42-+3H+
氯碱工业基础反应为电解饱和食盐水的反应,反应方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑,故D为NaOH;又因为B能与金属X反应,故B、C分别为Cl2、H2;联想Cl2能与Fe、Cu、Na等反应,若X为Fe(Cu),则E为FeCl3(CuCl2),F为Fe2O3(CuO);反应②为金属与金属氧化物在高温下发生的反应,应该是铝热反应,可推测Y为Al,则G为Al2O3,则I为NaAlO2。形成酸雨的主要气体为SO2和NOx,过量二氧化硫气体通入氢氧化钠溶液生成NaHSO3,NaAlO2溶液中通过量SO2气体也生成NaHSO3。若Z为NO2,NO2通入NaOH溶液生成NaNO3、NaNO2和H2O,题中H溶液中溶质只有一种,所以Z只能为SO2,H为NaHSO3。空气中含量最高的气体为N2,N2与H2反应方程式为N2+3H2
2NaOH+H2↑+Cl2↑,故D为NaOH;又因为B能与金属X反应,故B、C分别为Cl2、H2;联想Cl2能与Fe、Cu、Na等反应,若X为Fe(Cu),则E为FeCl3(CuCl2),F为Fe2O3(CuO);反应②为金属与金属氧化物在高温下发生的反应,应该是铝热反应,可推测Y为Al,则G为Al2O3,则I为NaAlO2。形成酸雨的主要气体为SO2和NOx,过量二氧化硫气体通入氢氧化钠溶液生成NaHSO3,NaAlO2溶液中通过量SO2气体也生成NaHSO3。若Z为NO2,NO2通入NaOH溶液生成NaNO3、NaNO2和H2O,题中H溶液中溶质只有一种,所以Z只能为SO2,H为NaHSO3。空气中含量最高的气体为N2,N2与H2反应方程式为N2+3H2 2NH3。反应②化学方程式为:2Al+Fe2O3
2NH3。反应②化学方程式为:2Al+Fe2O3 2Fe+Al2O3或2Al+3CuO
2Fe+Al2O3或2Al+3CuO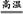 3Cu+Al2O3。Cl2具有氧化性,HS
3Cu+Al2O3。Cl2具有氧化性,HS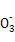 具有还原性,足量Cl2通入NaHSO3溶液中发生氧化还原反应,离子方程式为Cl2+HSO3-+H2O=2Cl-+SO42- +3H+。
具有还原性,足量Cl2通入NaHSO3溶液中发生氧化还原反应,离子方程式为Cl2+HSO3-+H2O=2Cl-+SO42- +3H+。
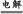 2NaOH+H2↑+Cl2↑,故D为NaOH;又因为B能与金属X反应,故B、C分别为Cl2、H2;联想Cl2能与Fe、Cu、Na等反应,若X为Fe(Cu),则E为FeCl3(CuCl2),F为Fe2O3(CuO);反应②为金属与金属氧化物在高温下发生的反应,应该是铝热反应,可推测Y为Al,则G为Al2O3,则I为NaAlO2。形成酸雨的主要气体为SO2和NOx,过量二氧化硫气体通入氢氧化钠溶液生成NaHSO3,NaAlO2溶液中通过量SO2气体也生成NaHSO3。若Z为NO2,NO2通入NaOH溶液生成NaNO3、NaNO2和H2O,题中H溶液中溶质只有一种,所以Z只能为SO2,H为NaHSO3。空气中含量最高的气体为N2,N2与H2反应方程式为N2+3H2
2NaOH+H2↑+Cl2↑,故D为NaOH;又因为B能与金属X反应,故B、C分别为Cl2、H2;联想Cl2能与Fe、Cu、Na等反应,若X为Fe(Cu),则E为FeCl3(CuCl2),F为Fe2O3(CuO);反应②为金属与金属氧化物在高温下发生的反应,应该是铝热反应,可推测Y为Al,则G为Al2O3,则I为NaAlO2。形成酸雨的主要气体为SO2和NOx,过量二氧化硫气体通入氢氧化钠溶液生成NaHSO3,NaAlO2溶液中通过量SO2气体也生成NaHSO3。若Z为NO2,NO2通入NaOH溶液生成NaNO3、NaNO2和H2O,题中H溶液中溶质只有一种,所以Z只能为SO2,H为NaHSO3。空气中含量最高的气体为N2,N2与H2反应方程式为N2+3H2 2NH3。反应②化学方程式为:2Al+Fe2O3
2NH3。反应②化学方程式为:2Al+Fe2O3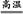 2Fe+Al2O3或2Al+3CuO
2Fe+Al2O3或2Al+3CuO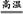 3Cu+Al2O3。Cl2具有氧化性,HS
3Cu+Al2O3。Cl2具有氧化性,HS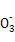 具有还原性,足量Cl2通入NaHSO3溶液中发生氧化还原反应,离子方程式为Cl2+HSO3-+H2O=2Cl-+SO42- +3H+。
具有还原性,足量Cl2通入NaHSO3溶液中发生氧化还原反应,离子方程式为Cl2+HSO3-+H2O=2Cl-+SO42- +3H+。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目