题目内容
在某密闭容器内有正反应为放热的可逆反应,其中A、B为气体,C为固体,若反应开始经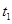 s后达平衡。如图:
s后达平衡。如图: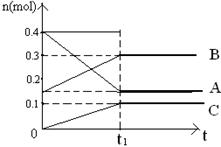
(1)该反应的化学方程式为_________________________
(2)反应物的转化率______________________
(3)要使反应物的转化率增加可能的原因是____________
A.增大了B或C的浓度 B.使用了催化剂
C.缩小体积,使体系压强增大 D.升高了反应温度
(4)该反应达到平衡后,向该容器中再充入0.5mol的He。若恒温恒压,,这时反应速率 _________(填“加快”、“减慢”或“不变”),平衡_____________ (填“向正方向移动”、“向逆方向移动”、“不移动”);若恒温恒容时,这时反应速率_______(填“加快”、“减慢”或“不变”),反应物的转化率___________(填“加快”、“减慢”或“不变”)。
(1) 5A=3B+2C (2)62. 5℅ (3)C (4)减慢 向逆反应方向移动。 不变 不变
解析试题分析:(1)由图可看出:A的物质的量从0.4mol—0.15mol,是反应物;B的物质的量从0.15mol—0.3mol,是生成物;C的物质的量从0—0.1mol,是生成物.这几种物质变化的物质的量之比为:0.25:0.15:0.1=5:3:2根据它们反应时物质的量的比等于化学方程式中该物质的计量数的比。又因为最终各种物质都存在,所以该反应是可逆反应。可得方程式:5A(g) 3B(g)+2C(s).(2)反应物A的转化率为:(0.25÷0.4)× 100%=62.5%。(3)该反应的正反应是个气体体积减小的放热反应,所以要使反应物的转化率增加,就要使平衡向正反应方向移动。而增大B或C的浓度平衡逆向移动。错误。B使用催化剂平衡不移动,对其转化率无影响。错误。C.缩小体积,使体系压强增大 ,能使平衡正反应方向移动,使A反应物的转化率增加。正确。D.升高了反应温度平衡逆反应方向移动,A反应物的转化率降低。错误。正确选项为:C。(4)该反应达到平衡后,若恒温恒压,向该容器中再充入0.5mol的He。容器的体积就扩大,反应物、生成物的浓度减小,这时反应速率减慢。由于反应物的浓度减小的多,所以平衡向逆反应方向移动。若恒温恒容时,因为反应混合物中各物质的浓度不变,平衡不移动。所以这时反应速率不变,反应物的转化率也不变。(
3B(g)+2C(s).(2)反应物A的转化率为:(0.25÷0.4)× 100%=62.5%。(3)该反应的正反应是个气体体积减小的放热反应,所以要使反应物的转化率增加,就要使平衡向正反应方向移动。而增大B或C的浓度平衡逆向移动。错误。B使用催化剂平衡不移动,对其转化率无影响。错误。C.缩小体积,使体系压强增大 ,能使平衡正反应方向移动,使A反应物的转化率增加。正确。D.升高了反应温度平衡逆反应方向移动,A反应物的转化率降低。错误。正确选项为:C。(4)该反应达到平衡后,若恒温恒压,向该容器中再充入0.5mol的He。容器的体积就扩大,反应物、生成物的浓度减小,这时反应速率减慢。由于反应物的浓度减小的多,所以平衡向逆反应方向移动。若恒温恒容时,因为反应混合物中各物质的浓度不变,平衡不移动。所以这时反应速率不变,反应物的转化率也不变。(
考点:考查

常温下按照如下方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是_____________________________________。
(2)实验①和②的目的是____________________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是____________________。
(3)写出实验③的化学反应方程式 。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。

分析上图能够得出的实验结论是______________________________________。
 N2O4已经达到平衡。
N2O4已经达到平衡。
 2SO3(g);△H=-196 kJ/mo1,850K时,在2L固定容积的密闭容器中充入2mol SO2和2mol O2,10分钟后达到平衡,SO2浓度和时间关系如图。
2SO3(g);△H=-196 kJ/mo1,850K时,在2L固定容积的密闭容器中充入2mol SO2和2mol O2,10分钟后达到平衡,SO2浓度和时间关系如图。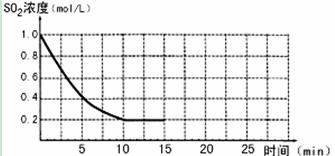
 cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示: 

 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图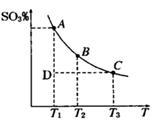 所示,根据图回答下列问题:
所示,根据图回答下列问题:
 ,据此回答以下问题:
,据此回答以下问题: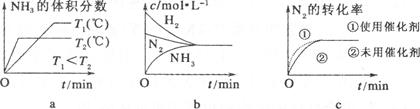
 pC达到平衡,若:
pC达到平衡,若: 2B(s) + 6HBr(g) 来制取晶体硼。完成下列填空:
2B(s) + 6HBr(g) 来制取晶体硼。完成下列填空: