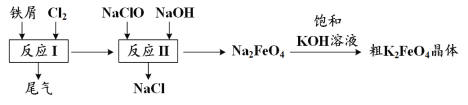��Ŀ����
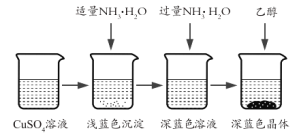
����Ŀ��п�̸ɵ���Ǻܹ��ϵ�һ���Ե�أ���������ԭ����Ҫ�����̿����п������Ա�������ۺ��������̿����п���ͬ��������գ�������������ͼ��ʾ��

��֪�����̿��к�MnO2Լ66%��SiO2Լ20%��Al2O3Լ4%������Ϊˮ�֣���п���к�ZnSԼ80%��FeS��CuS��SiO2��Լ7%������Ϊˮ�֡�
��ش��������⣺
��1����ӦI�費�Ͻ��裬��Ŀ����______________��
��2����ӦI����Ҫ��������ԭ��Ӧ��ѧ����ʽΪ______________��
��3�����鷴ӦI��Һ��Fe3+���Լ�Ϊ____________________����ӦIII��MnO2��������______________��
��4����֪Ksp��ZnCO3��=1.4��10-10��Ksp��MnCO3��=2.2��10-11��Ҫʹ��ӦIV֮�����Һ��Zn2+��Mn2+Ũ�Ⱦ�����1.0��10-6 mol��L-1������Һ�в�����CO32-Ũ������Ϊ___mol��L-1��
��5����ͼ��Na2SO4��Na2SO410H2O���ܽ������
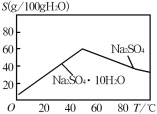
��g/100gˮ��������еõ�Na2SO4����IJ����ǣ��������MnCO3��ZnCO3�����Һ�����ᾧ��_______�� ���Ҵ�ϴ����������Ҵ�ϴ�Ӷ�����ˮϴ��ԭ����___________��
���𰸡��ӿ췴Ӧ���ʣ����ԭ�������� ZnS+MnO2+2H2SO4 =ZnSO4 +S+MnSO4+2H2O KSCN��Һ ��Fe2+������Fe3+ 1.4��10-4 ���ȹ��� ���Ҵ�ϴ�ӿ��Է�ֹNa2SO4����ת��ΪNa2SO410H2O������ֹNa2SO4������ˮ�����
��������
���̿���п���м����ᣬ��ӦI��ҪΪ��MnO2�������������ԭ��Ӧ����Mn2+��S��Fe3+��Al3+��Zn2+��Cu2+�ȣ����˳�ȥS��SiO2��
����Һ�м�����Zn������Ӧ��Zn��Cu2+��Fe3+��Ӧ����Cu��Fe2+��Zn2+�����˳�ȥCu����Һ������Ӧ��MnO2��Fe2+��Ӧ����Mn2+��Fe3+��ͨ����pHʹFe3+��Al3+�γɳ�����ȥ��
Zn2+��Mn2+��Na2CO3�ɷ�����Ӧ���õ�Na2SO4��MnCO3��ZnCO3�ṩ����Ӧ���ã�Ҳ�ɷ�����Ӧ�������MnO2��Zn���ݴ˷������
(1)��ӦI���Ͻ��裬���̿����п���ֽӴ���һ������Լӿ췴Ӧ���ʣ���һ�����ʹ���̿����п���ܷ�Ӧ�����ԭ�������ʣ��ʴ�Ϊ���ӿ췴Ӧ���ʣ����ԭ�������ʣ�
(2)���̿��еijɷ���ҪΪMnO2����п������Ҫ�ɷ�ΪZnS�����Է�ӦI����Ҫ����MnO2����ZnS�ķ�Ӧ�����ԭ���غ㡢���ӵ�ʧ�غ�ɵ÷���ʽΪ��ZnS+MnO2+2H2SO4 =ZnSO4 +S+MnSO4+2H2O���ʴ�Ϊ��ZnS+MnO2+2H2SO4 =ZnSO4 +S+MnSO4+2H2O��
(3)ͨ����KSCN��Һ����Fe3+��������ķ�����֪����ӦIII��MnO2�������ǽ�Fe2+������Fe3+���Ա��γɳ�������ȥ���ʴ�Ϊ��KSCN��Һ����Fe2+������Fe3+��
(4) Zn2+Ũ�Ƚ���1.0��10-6 mol��L-1������CO32-Ũ��=![]() mol��L-1=1.4��10-4 mol��L-1��Mn2+Ũ�Ƚ���1.0��10-6 mol��L-1������CO32-Ũ��=
mol��L-1=1.4��10-4 mol��L-1��Mn2+Ũ�Ƚ���1.0��10-6 mol��L-1������CO32-Ũ��=![]() mol��L-1=2.2��10-5 mol��L-1������������Ҫʹ��ӦIV֮�����Һ��Zn2+��Mn2+Ũ�Ⱦ�����1.0��10-6 mol��L-1������Һ�в�����CO32-Ũ������Ϊ1.4��10-4 mol��L-1���ʴ�Ϊ��1.4��10-4 ��
mol��L-1=2.2��10-5 mol��L-1������������Ҫʹ��ӦIV֮�����Һ��Zn2+��Mn2+Ũ�Ⱦ�����1.0��10-6 mol��L-1������Һ�в�����CO32-Ũ������Ϊ1.4��10-4 mol��L-1���ʴ�Ϊ��1.4��10-4 ��
(5)��Na2SO4��Na2SO410H2O���ܽ�����߿�֪���¶�̫�ͣ�Na2SO410H2O���ܽ�Ƚ�С���õ��Ĺ���ΪNa2SO410H2O����Ӧ�������MnCO3��ZnCO3�����Һ�����ᾧ�����ȹ��ˡ����Ҵ�ϴ�ӡ��������ˮϴ��ϴ�ӹ��̱�Ȼ�¶Ƚ��ͣ���һ����Na2SO4��ת��ΪNa2SO410H2O��ͬʱ��һ���ֻ�����ˮ����ˮ���ߣ������Ҵ�ϴ�ӿ��Է�ֹNa2SO4����ת��ΪNa2SO410H2O������ֹNa2SO4������ˮ����ģ��ʴ�Ϊ�����ȹ��ˣ����Ҵ�ϴ�ӿ��Է�ֹNa2SO4����ת��ΪNa2SO410H2O������ֹNa2SO4������ˮ����ġ�

 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�