��Ŀ����
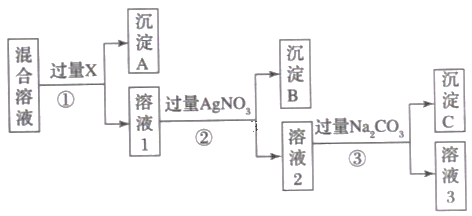
����Ŀ�����к�NaCl��Na2SO4��NaNO3�Ļ����Һ��ѡ���ʵ����Լ���ȥ��Һ�е�NaCl��Na2SO4���Ӷ��õ�������NaNO3��Һ����Ӧ��ʵ����̿�����ͼ��ʾ��
��ش��������⣺
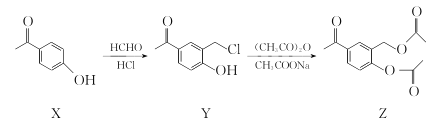
(1)�Լ�X����� ___________________(�ѧʽ)������X�Ƿ��������ķ�����____________��
(2)д����������Ӧ�����ӷ���ʽ��_______________________________________ ��д����������Ӧ�����ӷ���ʽ��____________________________________________ ��
(3)����ʵ�鷽���õ�����Һ3�п϶�����____________���ѧʽ����ͬ)������Ϊ�˳�ȥ�����ʣ���������Һ3�м��������____________��֮����Ҫ��ô�NaNO3���壬������е�ʵ�������_______________________________�����������)��
���𰸡�Ba(NO3)2 ��Һ���÷ֲ㣬�����μ�Ba(NO3)2 �����������ɣ���˵��Ba(NO3)2 �Ѿ�����������û�й��� Ag++Cl-��AgCl�� Ba2++CO32-=BaCO3����2Ag++CO32-=Ag2CO3�� Na2CO3 HNO3 ����
��������
������ͼ�Ͽ����ڢٲ�����ӦΪ��ȥ��Һ�е�SO42-����ʱ��Һ��������Ba2+���ڢڲ���������AgNO3��ӦΪ��ȥ��Һ�е�Cl-����ʱ��Һ��������Ag+���ڢ۲���������Na2CO3��ӦΪ��ȥ������Ba2+��Ag+����������CO32-��
(1)�Լ�XҪ�����ȳ���SO42-���־����ܲ������µ����ʣ�����ӦΪ�����Σ�����X�Ƿ��������ķ����Ǽ�������X�����Ƿ����ɳ�����
(2)�����������������Ȼ��Ƶ����ӷ�Ӧ����������Na2CO3��Ba2+��Ag+�ķ�Ӧ��
(3)����ʵ�鷽���õ�����Һ3�п϶�����Na2CO3������Ϊ�˳�ȥ�����ʣ���������Һ3�м�����������ᣬ֮����Ҫ��ô�NaNO3���壬������е�ʵ������Ǵ���Һ����ȡ���ʡ�
(1)�Լ�X�����Ba(NO3)2����Ϊ���ܱ�֤����SO42-�����ܱ�֤����������������ӡ�����X�Ƿ��������ķ����ǣ���Һ���÷ֲ㣬�����μ�Ba(NO3)2�����������ɣ���˵��Ba(NO3)2�Ѿ�����������û�й�����
�𰸣�Ba(NO3)2����Һ���÷ֲ㣬�����μ�Ba(NO3)2�����������ɣ���˵��Ba(NO3)2 �Ѿ�����������û�й�����
(2)�����ΪNaCl��AgNO3�ķ�Ӧ����Ӧ�����ӷ���ʽ��Ag++Cl-��AgCl��������۷���������Ӧ��һ���ǹ�����Ba2+��CO32-�ķ�Ӧ����һ����Ag+��CO32-�ķ�Ӧ����Ӧ�����ӷ���ʽΪBa2++CO32-=BaCO3����2Ag++CO32-=Ag2CO3����
�𰸣�Ag++Cl-��AgCl����Ba2++CO32-=BaCO3����2Ag++CO32-=Ag2CO3����
(3)����ʵ�鷽������Ϊ�����Na2CO3���������Եõ�����Һ3�п϶�����Na2CO3������Ϊ�˳�ȥ�����ʣ���������Һ3�м��������HNO3��֮����Ҫ��ô�NaNO3���壬������е�ʵ�������������
�𰸣�Na2CO3��HNO3��������

 �Ķ��쳵ϵ�д�
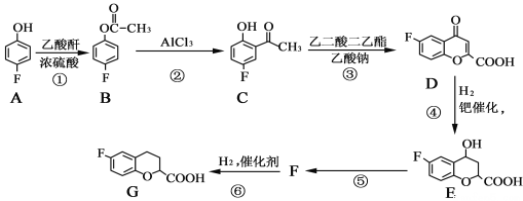
�Ķ��쳵ϵ�д�����Ŀ��������������C9H10O2������ˮ����ζ������������ˮ�㾫�����쾫�ͣ���������ʳƷ��ҵ�У�Ҳ�������л��ϳ��м��塢�ܼ��ȣ����Ʊ�����Ϊ��
![]() +C2H5OH
+C2H5OH![]()
![]() +H2O
+H2O
��֪��
��ɫ��״̬ | �е㣨�棩 | �ܶȣ�gcm��3�� | |
������* | ��ɫƬ״���� | 249 | 1.2659 |
���������� | ��ɫ����Һ�� | 212.6 | 1.05 |
�Ҵ� | ��ɫ����Һ�� | 78.3 | 0.7893 |
������ | ��ɫ����Һ�� | 80.8 | 0.7318 |
*��������100���Ѹ��������ʵ�鲽�����£�
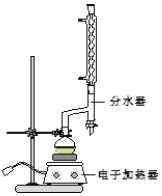
����Բ����ƿ�м���12.20g�����ᡢ25mL�Ҵ�����������20mL�����飬�Լ�4mLŨ���ᣬ��Ͼ��Ȳ������ʯ������ͼ��ʾװ�������������¶���6570����Ȼ���2h����Ӧʱ������һ�Ҵ���ˮ���γɡ���������е�62.6�棩��������������÷�ˮ�����Ϸ����ȥ��Ӧ���ɵ�ˮ��������������Ҵ���
�ڷ�Ӧ�������������ų���ˮ����Һ��ر��������������ȣ�����ˮ�����ռ�����Һ�岻���������ӣ�ֹͣ���ȣ�
�۽���ƿ�ڷ�ӦҺ����ʢ������ˮ���ձ��У���������Na2CO3����Һ�����ԣ�
���÷�Һ©���ֳ��л��㣬ˮ����25mL������ȡ��Һ��Ȼ��ϲ����л��㣮�����Ȼ��ƣ��Դֲ����������װ����ͼ��ʾ���������������Ѻ������£�����210213�����֣�
�ݼ���ϸ�ò�Ʒ���Ϊ13.16mL��
��1���ڸ�ʵ���У�Բ����ƿ���ݻ����ʺϵ���_____��������ȷѡ��ǰ����ĸ����
A.25mL B.50mL C.100mL D.250mL
��2��������з�ʯ��������____��ʹ�÷�ˮ�����Ϸ����ȥˮ��Ŀ����_____��
��3�������Ӧ������ֵ��¶���__��
A.215220�� B.8590�� C.7880�� D.6570��
��4������ۼ���Na2CO3��������________����Na2CO3���벻�㣬��֮������ʱ��������ƿ�пɼ����������ɣ������������ԭ����________��
��5�����ڲ�����е���ȡ��Һ����������ȷ����____��
A��ˮ��Һ�м������ѣ�ת������Һ©���У����ϲ���������Һ©����ת������������ҡ
B����ҡ���κ����Һ©���¿ڵIJ���������
C����������ҡ���������ֳַ�Һ©�����ô�Һ��ֲ�
D���ų�Һ��ʱ��Ӧ���Ͽڲ������������ϵİ��۶�©�����ϵ�С��
��6�����㱾ʵ��IJ���Ϊ____��