题目内容
2.在下列反应中,硫元素表现出氧化性的是( )| A. | 稀硫酸与锌反应 | B. | 二氧化硫与氧气反应 | ||
| C. | 浓硫酸与铜反应 | D. | 三氧化硫与水反应 |
分析 含元素化合价变化的反应为氧化还原反应,硫元素表现出氧化性,则硫元素的化合价降低,以此来解答.
解答 解:A.反应中Zn元素的化合价升高,H元素的化合价降低,不表现硫元素的氧化性,故A不选;
B.氧元素的化合价降低,S元素的化合价升高,故B不选;
C.Cu元素的化合价升高,S元素的化合价降低,则体现硫元素的氧化性,故C选;
D.反应中没有元素的化合价变化,不属于氧化还原反应,故D不选;
故选C.
点评 本题考查氧化还原反应,明确反应中元素的化合价变化为解答的关键,侧重氧化还原反应中氧化剂的考查,题目难度不大.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
12.某有机物的结构简式为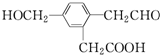 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )
①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去.
 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去.
| A. | ②③④ | B. | ①③④⑤⑥ | C. | ①③④⑤ | D. | ①③⑤⑥ |
13.下列叙述中能肯定说明金属A比金属B的活泼的是( )
| A. | A原子电子层数比B原子的电子层数多 | |
| B. | 常温时,A能从稀酸中置换出氢,而B不能 | |
| C. | A原子最外层电子数比B原子的最外层电子数少 | |
| D. | 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 |
10.有关电解质与非电解质的陈述,合理的是( )
| A. | 在水溶液中能导电的化合物都是电解质 | |
| B. | 在熔融状态下不导电的化合物都是非电解质 | |
| C. | 氨水为混合物,不属于电解质 | |
| D. | 硫酸溶于水能导电,所以浓硫酸为电解质 |
17.属于人工固氮作用的是( )
| A. | N2与H2在一定条件下反应生成NH3 | B. | 硝酸工厂用NH3氧化制NO | ||
| C. | 雷雨时空气中的N2转化为NO | D. | 由NH3制碳酸氢铵和硫酸铵 |
7.F、Cl和Br都是 VIIA族元素,关于这三种元素原子的说法正确的是( )
| A. | 原子半径:F>Cl>Br | B. | 最外层电子数都相同 | ||
| C. | 核外电子层数都相同 | D. | 最外层电子数依次增多 |
14.25℃时,下列有关溶液微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol/L CH3COONa与0.1 mol/L HCl溶液等体积混合:c(Na+)>c(Cl-)>cCH3COO-)>c(OH-) | |
| B. | 0.1mol/L NH4Cl与0.1mol/L 氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1mol/L Na2CO3与0.1mol/L NaHCO3溶液等体积混合:2c(Na+)=3c(HCO3-)+3c(CO32-)+3c(H2CO3) | |
| D. | 0.11 mol/L CH3COOH溶液与 0.1 mol/L NaOH溶液等体积混合,所的溶液中:c(OH-)>c(H+)+c(CH3COOH) |
11.向0.15mol Cu粉与Fe粉的混合物中加入一定量的稀硫酸产生气体XL,然后加入一定量的稀硝酸,充分反应后固体全部溶解,收集到NO气体Y L,(气体体积均已换算到标准状况).则X+Y的数值可能是( )
| A. | 1.12 | B. | 2.24 | C. | 2.8 | D. | 4.48 |
7.下列有关同分异构体数目的叙述中,正确的是( )
| A. | C5H12有2种同分异构体 | |
| B. | C8H10中只有三种属于芳香烃的同分异构体 | |
| C. | CH3CH2CH2CH3光照下与氯气反应,只生成一种一氯代烃 | |
| D. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |