题目内容
【题目】下列有关氢键的存在及类别的说法正确的是( )
A.氢键广泛存在于所有原子间B.氢键是一种极弱的化学键
C.氢键是一种重要的范德华力D.氢键既能存在于分子间,也能存在于分子内
【答案】D
【解析】
A.氢键仅存在于电负性较大的几种元素原子与H原子之间,A错误;
B.氢键不是化学键,B错误;
C.氢键与范德华力均属于分子间作用力,氢键不是一种重要的范德华力,C错误;
D.氢键既能存在于分子间,如H2O;氢键也能存在于分子内,如邻羟基苯甲醛,D正确;
答案选D。

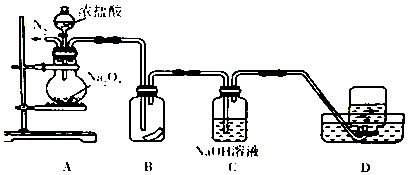
【题目】黄铁矿石的主要成分为FeS2和少量FeS(假设其他杂质中不含Fe、S元素,且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组对该黄铁矿石进行如下实验探究。将m1 g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全。其反应的化学方程式为:
![]()

【实验一】:测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:

①鼓入空气的作用是_________________________________。
②反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是(用化学方程式表示)________________________________________。
H2O2可以看作是一种很弱的酸,写出其电离方程式:_____________________。
(3)该黄铁矿石中硫元素的质量分数为______________(列出表达式即可)。
【实验二】:测定铁元素的含量

(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量____________(填“偏大”、“偏小”或“无影响”)。
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有_________________。
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 20.00 | 24.97 |
根据所给数据,计算该稀释液中Fe2+的物质的量浓度为c(Fe2+) =_______________。