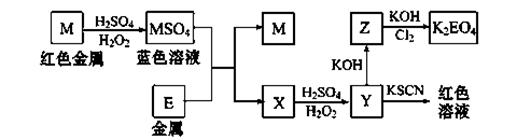
题目内容
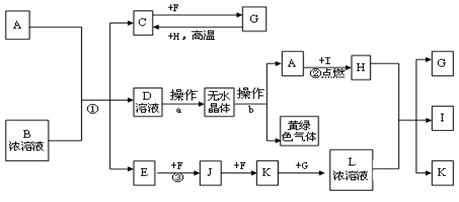
在一定条件下,单质B、C、D、E都能与A单质发生化合反应,转化关系如图所示。已知:①G是黑色晶体,能吸附B单质;②H能与氢氧化钠溶液或盐酸反应;③实验时在G和C的混合物表面加入某强氧化剂粉末,在表面上插入一根除去氧化膜的E片,点燃E引发G与C的反应;④I是绿色植物光合作用的原料,温室中常用它作肥料。根据上述信息,回答下列问题:
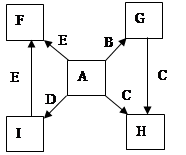

(1)I的电子式为 ,G的俗名是 。
(2)以C和E为电极在NaOH溶液中构成原电池,该原电池的负极反应式为 。
(3)根据E和A反应的能量变化图像写出热化学方程式: 。
(4)两种常见含C元素的盐,一种pH>7,另一种pH<7,写出这两种溶液混合时发生反应的离
子方程式:
(5)写出B在高温下和水蒸气反应的化学方程式并标出电子转移方向和总数 。
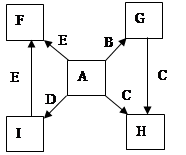

(1)I的电子式为 ,G的俗名是 。
(2)以C和E为电极在NaOH溶液中构成原电池,该原电池的负极反应式为 。
(3)根据E和A反应的能量变化图像写出热化学方程式: 。
(4)两种常见含C元素的盐,一种pH>7,另一种pH<7,写出这两种溶液混合时发生反应的离
子方程式:
(5)写出B在高温下和水蒸气反应的化学方程式并标出电子转移方向和总数 。
(1)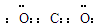 (1分), 磁性氧化铁(1分)
(1分), 磁性氧化铁(1分)
(2) Al-3e-+4OH-= AlO2-+2H2O (2分)
(3)2Mg(s)+O2(g)=2MgO(s) △H = -10QkJ/mol(2分)
(4)3AlO2-+Al3++6H2O = 4Al(OH)3↓(2分)
(5) (2分)
(2分)
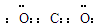 (1分), 磁性氧化铁(1分)
(1分), 磁性氧化铁(1分) (2) Al-3e-+4OH-= AlO2-+2H2O (2分)
(3)2Mg(s)+O2(g)=2MgO(s) △H = -10QkJ/mol(2分)
(4)3AlO2-+Al3++6H2O = 4Al(OH)3↓(2分)
(5)
 (2分)
(2分)试题分析:根据题意和转化关系图分析:①G是黑色晶体,能吸附B单质,则G为Fe3O4,B为Fe,A为O2,②H能与氢氧化钠溶液或盐酸反应;H为两性氧化物氧化铝,C为铝;③实验时在G和C的混合物表面加入某强氧化剂粉末,在表面上插入一根除去氧化膜的E片,点燃E引发G与C的反应;为铝热反应的引发操作,E为镁,F为氧化镁;④I是绿色植物光合作用的原料,I为二氧化碳,D为碳;(1)I为CO2,电子式为
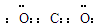 ,G为四氧化三铁,俗名是磁性氧化铁;(2)以铝和镁为电极在NaOH溶液中构成原电池,铝与NaOH溶液反应,作原电池的负极,该原电池的负极反应式为Al-3e-+4OH-= AlO2-+2H2O;(3)根据能量变化图像可写出镁和氧气反应的热化学方程式:2Mg(s)+O2(g)=2MgO(s) △H = -10QkJ/mol;(4)两种常见含铝元素的盐,一种pH>7,为偏铝酸盐,另一种pH<7,为铝盐,两种溶液混合时发生反应的离子方程式为3AlO2-+Al3++6H2O = 4Al(OH)3↓;(5)铁在高温下和水蒸气反应的化学方程式及电子转移方向和总数为
,G为四氧化三铁,俗名是磁性氧化铁;(2)以铝和镁为电极在NaOH溶液中构成原电池,铝与NaOH溶液反应,作原电池的负极,该原电池的负极反应式为Al-3e-+4OH-= AlO2-+2H2O;(3)根据能量变化图像可写出镁和氧气反应的热化学方程式:2Mg(s)+O2(g)=2MgO(s) △H = -10QkJ/mol;(4)两种常见含铝元素的盐,一种pH>7,为偏铝酸盐,另一种pH<7,为铝盐,两种溶液混合时发生反应的离子方程式为3AlO2-+Al3++6H2O = 4Al(OH)3↓;(5)铁在高温下和水蒸气反应的化学方程式及电子转移方向和总数为 。
。
练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目