题目内容
【题目】亚硝酸钠(NaNO2)是一种重要的工业盐,易溶于水,微溶于乙醇。某化学兴趣小组对亚硝酸钠进行多角度探究:
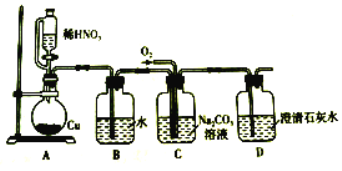
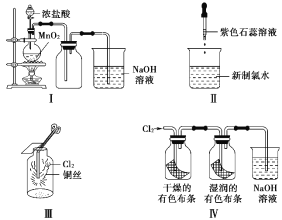
Ⅰ.亚硝酸钠的制备。
(1)装置B的作用是________________________。
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的离子方程式为______________。
Ⅱ.探究亚硝酸钠与硫酸反应![]() 气体产物成分。
气体产物成分。
已知:①NO+NO2+2OH-=2NO+H2O
②气体液化的温度:NO2为21 ℃,NO为-152 ℃
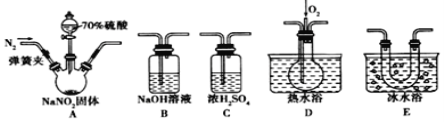
(3)反应前应打开弹簧夹,先通入一段时间氮气,目的是_______________________。
(4)仪器的连接顺序(按左→右连接):A→C→________。
(5)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,装置A中产生红棕色气体。若D中通入过量O2,装置B中的化学方程式是_______________________。
Ⅲ.设计实验证明酸性条件下NaNO2具有氧化性。
(6)供选用的试剂:NaNO2溶液、KMnO4溶液、Fe2(SO4)3溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液___________________________________________________。
【答案】除去HNO3 4NO+O2+2CO32-=4NO2-+2CO2 排尽空气,防止可能生成的NO被完全氧化成NO2,造成对A中反应产物检验的干扰 E→D→B 4NO2+O2+4NaOH=4NaNO3+2H2O 取碘化钾溶液并滴加稀硫酸酸化,滴加淀粉溶液,无明显现象,滴加少许NaNO2溶液,溶液变蓝,证明NaNO2具有氧化性
【解析】
(1)硝酸易挥发,所以装置B的作用是除去HNO3;
(2)N元素化合价升高,必有O2参与,同时澄清石灰水变浑浊,有CO2生成,反应方程式为:4NO+O2+2CO32-=4NO2-+2CO2;
(3)空气中的氧气能氧化NO,所以必须先排尽空气,防止可能生成的NO被完全氧化成NO2,造成对A中反应产物检验的干扰;
(4)由于NO2的液化温度高,所以首先检验NO2,即先通过E,然后再通过D,最后需要有尾气处理;
(5)若氧气过量,则进入B装置的气体全部是NO2,所以反应的方程式为:4NO2+O2+4NaOH=4NaNO3+2H2O;
(6)取碘化钾溶液并滴加稀硫酸酸化,滴加淀粉溶液,无明显现象,滴加少许NaNO2溶液,溶液变蓝,证明NaNO2具有氧化性。
Ⅰ.(1)硝酸易挥发,所以装置B的作用是除去HNO3,故答案为:除去HNO3。
(2)N元素化合价升高,必有O2参与,同时澄清石灰水变浑浊,有CO2生成,则C中制备NaNO2的离子方程式为:4NO+O2+2CO32-=4NO2-+2CO2,故答案为:4NO+O2+2CO32-=4NO2-+2CO2。
Ⅱ.(3)空气中的氧气能氧化NO,所以必须先排尽空气,防止可能生成的NO被完全氧化成NO2,造成对A中反应产物检验的干扰,故答案为:排尽空气,防止可能生成的NO被完全氧化成NO2,造成对A中反应产物检验的干扰。
(4)由于NO2的液化温度高,所以首先检验NO2,即先通过E,然后再通过D,最后需要有尾气处理,即连接顺序是E→D→B,故答案为:E→D→B。
(5)若氧气过量,则进入B装置的气体全部是NO2,所以反应的方程式为:4NO2+O2+4NaOH=4NaNO3+2H2O,故答案为:4NO2+O2+4NaOH=4NaNO3+2H2O。
Ⅲ.(6)取碘化钾溶液并滴加稀硫酸酸化,滴加淀粉溶液,无明显现象,滴加少许NaNO2溶液,溶液变蓝,证明NaNO2具有氧化性,故答案为:取碘化钾溶液并滴加稀硫酸酸化,滴加淀粉溶液,无明显现象,滴加少许NaNO2溶液,溶液变蓝,证明NaNO2具有氧化性。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案