题目内容
现有ag CH4在足量的氧气中充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加( )
| A、a g | B、1.5a g |
| C、2a g | D、2.5a g |
考点:钠的重要化合物,化学方程式的有关计算
专题:计算题
分析:CH4在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应,
发生2CO+O2
2CO2、2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
发生2H2+O2
2H2O、H2O+2Na2O2=4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知反应后固体增加的质量为氢气质量,以此解答该题.
发生2CO+O2
| ||
发生2H2+O2
| ||
解答:
解:CH4在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应,
发生2CO+O2
2CO2、2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
发生2H2+O2
2H2O、H2O+2Na2O2=4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知反应后固体增加的质量为氢气质量,
ag CH4的物质的量为
mol,可生成
molCO2,
mol H2O,相当于m(CO)+m(H2)=
mol×28+
mol×2=2a,
则固体的质量增大2ag.
故选C.
发生2CO+O2
| ||
发生2H2+O2
| ||
ag CH4的物质的量为
| a |
| 16 |
| a |
| 16 |
| a |
| 8 |
| a |
| 16 |
| a |
| 8 |
则固体的质量增大2ag.
故选C.
点评:本题考查钠的重要化合物的性质,侧重于学生的分析能力和计算能力的考查,注意把握反应方程式的书写以及反应规律,为解答该题的关键,注意利用差量法进行判断,难度中等.

练习册系列答案
相关题目
下列说法中不正确的是( )
| A、纯净物一定由分子构成 |
| B、由同种分子构成的物质一定是纯净物 |
| C、混合物肯定是由两种以上的元素组成的 |
| D、只含一种元素的物质不一定是纯净物 |
将金属钠分别投入下列物质的水溶液中,产生气体和蓝色沉淀的是( )
| A、NaCl |
| B、K2SO4 |
| C、CuCl2 |
| D、MgCl2 |
关于溶液的下列说法正确的是( )
| A、用湿润的pH试纸测稀碱液的pH,测定值偏大 |
| B、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
| C、已知:H2B?H++HB-,HB-?H++B2-(电离常数K1=1.3×10-7,K2=7.1×10-15),则NaHB溶液显酸性 |
| D、除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
下列物质中,水解的最终产物含有葡萄糖的是( )
| A、油脂 | B、蛋白质 | C、蔗糖 | D、酶 |
将①氢气;②氧气;③甲烷三种气体分别盛放在三个容器中,并保持三个容器内气体的温度和密度均相等,这三种气体压强的大小关系是( )
| A、①>②=③ |
| B、①>③>② |
| C、①<②<③ |
| D、①<③<② |
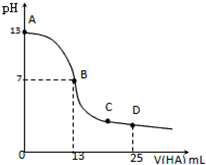 常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).下列说法错误的是( )
常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).下列说法错误的是( )| A、MOH的电离方程式为MOH=M++OH- |
| B、MOH与HA恰好完全反应时,溶液呈碱性,理由是A-+H2O=HA+OH-;此时,混合溶液中由水电离出的c(H+)大于0.2mol/L HA溶液中由水电离出的c(H+) |
| C、混合溶液中在B点:c(M+)=c(A-)>c(H+)=c(OH-);在C点:c(A-)>c(M+)>c(H+)>c(OH-) |
| D、溶液中D点时 c(A-)+c(HA)=2c(M+);若此时测得pH=3,则c(HA)+c(H+)=0.05+10-11mol/L |
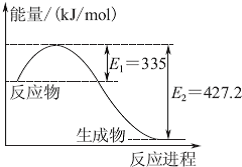 (1)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
(1)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol