题目内容
某兴趣小组设计如下装置进行氯气与金属钠的反应,先将钠预热,在钠熔融成小球时,撤火,并通入氯气即发生反应,下列叙述中错误的是
| A.钠着火剧烈燃烧产生苍白色的火焰 |
| B.反应产生的大量白烟是氯化钠固体 |
| C.棉球①的作用是吸收过量氯气防止产生污染 |
| D.棉球②变蓝色则证明氯气未被碱液完全吸收 |
A
解析试题分析:A.钠着火燃烧产生黄色火焰,故A错误;B.氯气性质活泼,易与活泼金属钠发生化合反应生成NaCl,反应时有大量白烟,故B正确;C.氯气有毒,不能排放到空气中,氯气易与NaOH溶液反应而被吸收,故C正确;D.氯气具有强氧化性,与碘化钾发生置换反应,可根据其颜色变化判断氯气是否被碱液完全吸收,棉球②变蓝色则证明氯气未被碱液完全吸收,不变蓝证明吸收完全,故D正确;故选A.
考点:本题考查氯气的性质,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的实验方案不合理的是( )
| A.取a克混合物充分加热,减重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
下列有关金属元素及其化合物说法不正确的是
| A.铁和氯气反应生成三价铁,和盐酸反应生成亚铁离子 |
| B.铜在潮湿的空气中易生锈呈绿色,锈的主要成分是碱式碳酸铜 |
| C.过氧化钠和氧化钠均可以与水、二氧化碳反应,但生成的产物不完全相同 |
| D.等质量的铝分别与足量的酸和碱溶液反应,生成气体的体积一定相同 |
金属钠着火时,可用来灭火的是
| A.二氧化碳 | B.水 | C.煤油 | D.沙土 |
NaCl是一种化工原料,可以制备一系列物质(如图所示)。下列说法正确的是( )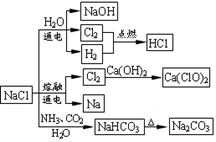
| A.石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂 |
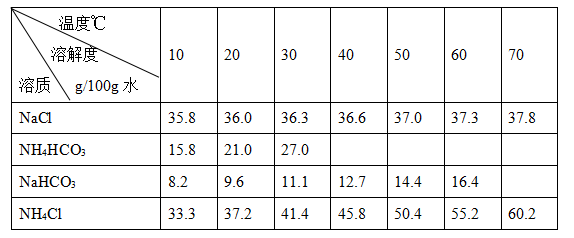
| B.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| C.常温下干燥Cl2能用钢瓶贮运,所以Cl2与铁不反应 |
| D.图中所示转化反应都是氧化还原反应 |
(12分)某小组进行铝热反应实验,装置如图所示。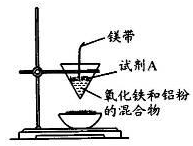
(1)铝热反应原理____(写化学方程式);试剂A为____(写化学式).实验现象____、有黑色固体生成。
(2)对黑色固体物质的组成,小组进行了如下探究
假设I该黑色物质为铁
假设Ⅱ该黑色物质为铁与四氧化三铁的混合物
【设计方案并实验】
| 实 验 步 骤 | 现 象 | 结 论 |
| ①取少量黑色固体于试管中加稀盐酸 | 固体全部溶解,有气泡产生 | 假设I成立,假设Ⅱ不成立 |
| ②滴入几滴0.01mol/LKSCN溶液 | 溶液不变色 |
你认为上述结论是否合理,__ __理由是__ __。
(3)取上述实验所得溶液,滴人适量氯水溶液变红色。此时涉及的离子反应方程式为
__ __、__ __;
利用反应体系中存在的平衡,小组再将溶液均分置于两支试管中并分别编号l、2.进行
如下探究:
| 实验编号 | 实验步骤 |
| 1 | ①滴加饱和FeCl3溶液4滴,充分振荡 |
| ②滴加几滴NaOH溶液 | |
| | ①滴加4滴1mol/LKSCN溶液 |
| ②滴加几滴NaOH溶液 |
主要探究的问题是__ __;
应重点观察的现象是__ __
预计得出的结论是__ __。