题目内容
甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油。
已知:①CH4 (g) + H2O (g)= CO (g)+3H2 (g) △H1=+206.2kJ·mol-1
② CH4(g)+ O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
③CH4 (g) + 2H2O (g) =CO2 (g) +4H2 (g) △H3="+165.0" kJ·mol-1
(1)CH4(g)与CO2 (g)反应生成CO(g)和H2(g)的热化学方程式为 。
(2)从原料选择和能源利用角度,比较方法①和②,为合成甲醇,用甲烷制合成气的适宜方法为 (填序号),其原因是 。
(3)合成气中的H2可用于生产NH3,在进入合成塔前常用Cu(NH3)2Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:
Cu(NH3)2Ac + CO + NH3 [Cu(NH3)3]Ac·CO △H<0
[Cu(NH3)3]Ac·CO △H<0
Cu(NH3)2Ac溶液吸收CO的适宜生产条件应是 。
(4)将CH4设计成燃料电池,其利用率更高,装置示意如右图(A、B为多孔性碳棒)。持续通入甲烷,在标准状况下,消耗甲烷体积VL。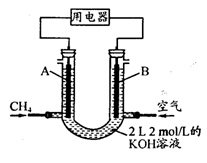
① 0<V≤44.8 L时,电池总反应方程式为 ;
② 44.8 L<V≤89.6 L时,负极电极反应为 ;
③ V="67.2" L时,溶液中离子浓度大小关系为 。
(14分)(1)CH4 (g)+CO2 (g)=2CO (g)+2H2 (g) △H="+247.4" kJ·mol-1(2分)
(2)②(2分) 选择CH4不完全燃烧制合成气时,放出热量,同时得到的CO、H2物质的量之比为1∶2,能恰好完全反应合成甲醇(2分)
(3)低温、高压(2分)
(4)①CH4 +2O2 +2KOH=K2CO3+3H2O(2分)
②CH4—8e-+ 9CO32-+3H2O=10HCO3-(2分)
③c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) (2分)
解析试题分析:(1)根据盖斯定律,①×2—③可约去H2O(g),则CH4(g)+CO2 (g)=2CO(g)+2H2(g)的△H=①的△H×2—③的△H=[(+206.2)×2—(+165.0)] kJ·mol-1="+247.4" kJ·mol-1;(2)从能量角度比较,①是吸热反应,需要消耗更多能量,②是放热反应,不需要太多能量;从原子利用率角度,由于CO+2H2→CH3OH,①的产物中氢原子不可能全部变为CH3OH,而②的产物中所有原子都可能全部变为CH3OH;因此选②,甲烷不完全燃烧制合成气时放出热量,还得到物质的量之比为1∶2的CO和H2的混合气体,能恰好完全反应生成甲醇;(3)由于正反应是气态物质体积减小的放热反应,因此采用降低温度、增大压强能使平衡右移,提高CO的转化率,防止催化剂中毒;(4)n(KOH)=2mol/L×2L=4mol,可能先后发生反应①CH4+2O2→CO2+2H2O、②CO2+2KOH=K2CO3+H2O、③K2CO3+CO2+H2O =2KHCO3;当0<V≤44.8 L时,0<n(CH4)≤2mol,则0<n(CO2)≤2mol,只发生反应①②,且KOH过量,则电池总反应式为CH4+2O2+2KOH=K2CO3+3H2O,负极反应式为CH4—8e—+10OH—=CO32—+7H2O;当44.8 L<V≤89.6 L,2mol <n(CH4)≤4mol,则2mol <n(CO2)≤4mol,发生反应①②③,得到K2CO3和KHCO3溶液,则负极反应式为CH4—8e—+ 9CO32—+3H2O =10HCO3—;当V="67.2" L时,n(CH4)=3mol,n(CO2)=3mol,则电池总反应式为3CH4+6O2+4KOH=K2CO3+2KHCO3+7H2O,则得到1mol K2CO3和2mol KHCO3的溶液,则c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)。
考点:考查化学反应运力,涉及运用盖斯定律计算焓变、热化学方程式的书写、评价物质合成方案、影响化学平衡的因素、燃料电池、溶液中离子浓度大小关系等重要考点。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
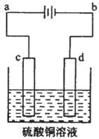
小学生10分钟应用题系列答案如下图装置所示,是用氢氧燃料电池B进行的某电解实验:
(1)若电池B使用了亚氨基锂(Li2NH)固体作为储氢材料,其储氢原理是:
Li2NH+H2=LiNH2+LiH ,则下列说法中正确的是 。
| A.Li2NH中N的化合价是-1 |
| B.该反应中H2既是氧化剂又是还原剂 |
| C.Li+和H+的离子半径相等 |
| D.此法储氢和钢瓶储氢的原理相同 |
① 若用固体Ca(HSO4)2为电解质传递H+,则电子由 极流出,H+向 极移动。(填“a”或“b ”)
② b极上的电极反应式为:
③ 外电路中,每转移0.1 mol电子,在a极消耗 L的H2(标准状况下)。
(3)若A中X、Y都是惰性电极,电解液W是滴有酚酞的饱和NaCl溶液,则B工作时:
① 电解池中X极上的电极反应式是 。在X极这边观察到的现象是 。
② 检验Y电极上反应产物的方法是 。
③ 若A中其它均不改变,只将电极Y换成铁棒,可实现的实验目的是 。
某小分子抗癌药物的分子结构如图所示,下列说法正确的是( )
| A.1mol该有机物最多可以和5mol NaOH反应 |
| B.该有机物容易发生加成、取代、中和、消去等反应 |
| C.该有机物遇FeCl3溶液不变色,但可使酸性KMnO4溶液褪色 |
| D.1mol该有机物与浓溴水反应,最多消耗3mol Br2 |






 Zn电池,它用不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极壳一端填充Ag2O和少量石墨组成的正极活性材料,负极盖一端填充Zn
Zn电池,它用不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极壳一端填充Ag2O和少量石墨组成的正极活性材料,负极盖一端填充Zn