题目内容
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol液态 H2O2混合恰好完全反应,生成氮气和水蒸气,放出256 kJ的热量。
(1)反应的热化学方程式为 。
(2)又已知16g液态肼与液态双氧水反应生成液态水时放出的热量是408 kJ。则H2O(g)=H2O(l)
的ΔH= 。
(3)已知N2(g) + 2O2(g) == 2NO2(g);△H=+67.7KJ/mol,
N2H4(g) + O2(g) == N2(g)+2H2O(g);△H= —534KJ/mol,
则肼与NO2完全反应的热化学方程式为_____ _____________________。
(1)反应的热化学方程式为N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)ΔH=-640 kJ·mol-1。
(2)ΔH=-44 kJ·mol-1。
(3)2N2H4(g) + 2NO2(g) == 3N2(g)+4H2O(g);△H= —1135.7KJ/mol,

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案仅用下表提供的实验操作或玻璃仪器(非玻璃仪器任选)就能够达到相应实验目的的是( )
| 选项 | 实验操作或玻璃仪器 | 实验目的 |
| A | 酸式滴定管、碱式滴定管、烧杯、锥形瓶 | 用0.01 mol/L的稀盐酸标定未知NaOH溶液的浓度 |
| B | 分液漏斗、锥形瓶、干燥管、导管、集气瓶 | 用碱石灰和浓氨水制备少量NH3 |
| C | 将浓硫酸和碳混合加热,直接将生成的气体通入足量的石灰水中,石灰水变浑浊 | 检验气体产物中CO2的存在 |
| D | 向某溶液中加入BaCl2溶液,产生白色沉淀 | 检验SO |
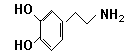 ⑴试判断多巴胺能发生的化学反应 。
⑴试判断多巴胺能发生的化学反应 。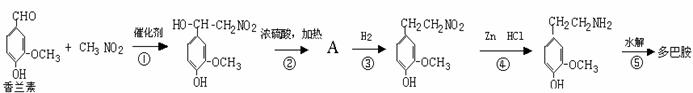 ⑶多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得。合成过程表示如下:
⑶多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得。合成过程表示如下:
 的存在
的存在