题目内容
某溶液中存在较多的H+、SO42-、NO3-,还可能大量存在的离子组是
| A.Al3+、CO32-、Cl- | B.Na+、NH4+、Cl- |
| C.Mg2+、Cl-、Fe2+ | D.Mg2+、Ba2+、Br- |
B
解析试题分析:离子间如果发生化学反应则不能大量共存,反之是可以的。A、H+与CO32-在溶液中反应生成CO2不能大量共存,A不正确;B、Na+、NH4+、Cl-、H+、SO42-、NO3-之间不反应可以大量共存,B正确;C、硝酸氧化亚铁离子不能大量共存,C不正确;D、Ba2+、SO42-反应生成硫酸钡沉淀不能大量共存,D不正确,答案选B。
考点:考查离子共存的正误判断

练习册系列答案
相关题目
下列解释事实的离子方程式不正确的是
A.氯化铜溶液显酸性:Cu2++2H2O Cu(OH)2+2H+ Cu(OH)2+2H+ |
| B.氯气使湿润的淀粉KI试纸变蓝:Cl2+2I-="2" Cl-+I2 |
| C.向硫酸铝溶液中加入氨水出现白色胶状沉淀:Al3++3OH-=Al(OH)3↓ |
| D.实验室不用玻璃塞试剂瓶盛装氢氧化钠溶液:SiO2+2 OH-= SiO32-+H2O |
解释下列事实的方程式不正确的是
| A.次氯酸钙溶液中通入过量二氧化硫:Ca2+ + 2ClO-+ H2O + SO2=CaSO3↓+ 2HClO |
| B.硫酸型酸雨放置一段时间溶液的pH下降:2H2SO3+O2=2H2SO4 |
C.纯碱液可以清洗油污的原因:CO32¯+H2O HCO3¯+OH¯ HCO3¯+OH¯ |
D.向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2O72—+H2O 2CrO42—+2H+ 2CrO42—+2H+ |
某澄清、透明的浅黄色溶液中,可能含有下列八种离子:Na +、NH4+、Fe3+、Ba2+、Al3+ 、SO42-、HCO3- 、I-,在设计检验方案前的初步分析中,可确定该溶液中能大量存在的离子最多有( )
| A.4种 | B.5种 | C.6种 | D.7种 |
下列事实、离子方程式及其对应关系均正确的是:
| A.铁溶于稀硝酸,溶液变为浅绿色:Fe + 4H+ + NO3—= Fe3+ + NO ↑ + 2H2O |
B.向K2Cr2O7溶液中滴加少量浓H2SO4,溶液变为黄色: Cr2O72-(橙色) + H2O  2CrO42-(黄色) +2H+ 2CrO42-(黄色) +2H+ |
| C.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H+ + 4I- + O2 =2I2 + 2H2O |
D.向水杨酸(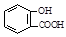 )中滴加NaHCO3溶液,放出无色气体: )中滴加NaHCO3溶液,放出无色气体: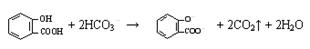 |
一包白色粉末,由几种常见的盐混合组成,其中只可能含有Na+、K+、Al3+、 、
、 、
、 、
、 、
、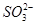 中的若干种离子。某同学对该溶液进行如下实验:
中的若干种离子。某同学对该溶液进行如下实验: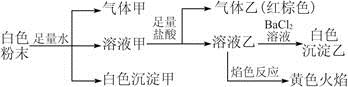
以下说法正确的是
A.白色沉淀甲是Al(OH)3,气体甲是CO2,所以混合物一定含Al3+和 |
| B.气体乙一定是NO和NO2的混合气体 |
C.白色沉淀乙是BaSO4,所以原混合物一定含有 |
| D.焰色反应为黄色火焰,不能确定原混合物中不含K+ |
下列化学反应的离子方程式书写正确的是( )。
| A.稀硝酸和过量铁屑反应:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| B.向硫酸氢铵溶液中加入少量氢氧化钠溶液:NH4++OH-=NH3↑+H2O |
| C.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| D.H2C2O4使酸性KMnO4溶液褪色:5H2C2O4+6H++2MnO4-=10CO2↑+2Mn2++8H2O |
下列有关的离子方程式中正确的是( )
| A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4+ |
B.铜片接电源正极,碳棒接电源负极,电解硫酸溶液:Cu+2H+ Cu2++H2↑ Cu2++H2↑ |
C.磷酸一氢钠溶液水解:HPO42-+H2O PO43-+H3O+ PO43-+H3O+ |
| D.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O=4Fe3++4OH- |