��Ŀ����
����Ŀ��ijѧϰС��̽��Ũ��ϡ���������Ե����ǿ���ģ�����ͼװ�ý������飨�г���������ȥ����ʵ�����Ũ�����ܽ�![]() ������
������![]() ����ϡ���������
����ϡ���������![]() ���ɴ˵ó��Ľ�����Ũ�����������ǿ��ϡ���ᡣ
���ɴ˵ó��Ľ�����Ũ�����������ǿ��ϡ���ᡣ
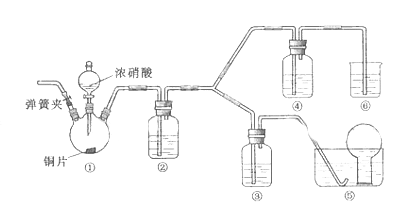
��ѡҩƷ��Ũ���ᡢ3mo/Lϡ���ᡢ����ˮ��Ũ���ᡢ����������Һ��������̼
��֪������������Һ����![]() ��Ӧ������
��Ӧ������![]() ��Ӧ
��Ӧ
![]()
��1�� ʵ��Ӧ�����к������ŷŵ������У�װ�âۡ��ܡ����г˷ŵ�ҩƷ������
��2�� �μ�Ũ����֮ǰ�IJ���ʱ����װ�õ������ԣ�����ҩƷ�����ɼк�
��3�� װ�â��з�����Ӧ�Ļ�ѧ����ʽ��
��4�� װ�âڵ������� ��������Ӧ�Ļ�ѧ����ʽ��
��5�� ��С��ó��Ľ���һ�ֵ�����������
��6�� ���������ͬѧ�Ƿ���װ�â�����Һ����ɫ����������ɫ����ͬѧ��Ϊ�Ǹ���Һ������ͭ�����������ϸ����£�����ͬѧ��Ϊ�Ǹ���Һ���ܽ������ɵ����塣ͬѧ�Ƿֱ��漰��һ��4���������ж����ֿ����Ƿ���ȷ����Щ�����п��е��� ��ѡ�������ĸ��
a. ���ȸ���ɫ��Һ���۲���ɫ�仯
b. ��ˮϡ����ɫ��Һ���۲���ɫ�仯
c. �����ɫ��Һ��ͨ�뵪�����۲���ɫ�仯
d. ������ͭ��Һ��ͨ��Ũ������ͭ��ӳ���������壬�۲���ɫ�仯
���𰸡���1��3mol/Lϡ���ᡢŨ���ᡢ����������Һ
��2��ͨ��CO2һ��ʱ�䣬�رյ��ɼУ���װ�â��е���ĩ�����뵹�õ���ƿ��
�� 3��Cu + 4HNO3��Ũ��= Cu(NO3)2 + 2NO2�� + 2H2O
��4����NO2ת��ΪNO 3NO2 + H2O =2HNO3 + NO
��5��װ�â���Һ���Ϸ�������Ϊ��ɫ��װ�â���Һ���Ϸ���������ɫ��Ϊ����ɫ
��6��a c d
��������
�����������1������װ���ص��ʵ��Ŀ�ģ�װ�â����ռ�NO��װ�â���ʢ��NaOH��Һ����NO2��ֹ��Ⱦ��������ΪҪ��֤ϡHNO3��������NO������װ�â���Ӧ��ʢ��ϡ���ᣮװ�âۡ��ܡ����г˷ŵ�ҩƷ������3mol/Lϡ���ᡢŨ���ᡢ����������Һ��2������װ���вд�Ŀ���������NO����ʵ��������ţ����Եμ�ŨHNO3֮ǰ��Ҫͨ��һ��ʱ��CO2����װ���еĿ�����ͬʱҲ�轫װ�â��е���ĩ�����뵹�õ���ƿ�ڷ�ֹ��Ӧ������NO�����ݳ�����3��װ�â��з�����Ӧ�Ļ�ѧ����ʽ����
Cu + 4HNO3��Ũ��= Cu(NO3)2 + 2NO2�� + 2H2O��
��4��װ�â���ʢ��H2O��ʹNO2��H2O��Ӧ����NO��3NO2+H2O=2HNO3+NO�� ��5��NOͨ��ϡHNO3��Һ��������ɫNO2������˵��ϡHNO3��������NO������ʢ��ϡHNO3װ�õ�Һ���Ϸ�û����ɫ�仯����˵��֮��װ�â���ʢ�ŵ���ŨHNO3����ŨHNO3������NO��װ�â�Һ����Ϸ����������ɫ���壮��s��Ҫ֤����Cu��NO3��2Ũ�ȹ������ܽ���NO2����װ�â�����Һ����ɫ��һ�ǿ���ƽ��ܽ��NO2���ߣ�a��c�������ٹ۲���ɫ�仯������������Һ��Cu��NO3��2��Һ��Ũ�ȣ�d�������۲췴Ӧ�����ɫ�仯

����Ŀ����2016����ɽ��ģ������������һ�ֹ�ҵ�Σ������ʳ�ηdz����ƣ����Խ�ǿ��ij��ѧ��ȤС���ʳ�����������ƽ��ж�Ƕ�̽����
��һ������NaCl��NaNO2
��ͬѧ�ó���������
���飺������Ksp(AgNO2)=2��10-8�� Ksp(AgCl)=1.8��10-10���ֱ���ʢ��5mL 0.0001 mol/L��������Һ���Ժ���ͬʱ��εμ�0.0001mol/L��������Һ�������ɳ�������װ�� ��Һ���Թܡ�
��ͬѧ�ඨ��ҺpH
��pH��ֽ�ֱ�ⶨ0.1 mol/L��������Һ��pH�����NaNO2��Һ�ʼ��ԡ�����Һ�ʼ��Ե�ԭ���� �������ӷ���ʽ���ͣ���
��������С��������װ�ã���ȥ�г��������Ʊ���������
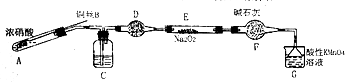
��֪���� 2NO+ Na2O2 = 2NaNO2 ��
�� ���������£�NO��NO2������MnO4һ��Ӧ����NO3һ��Mn2+��
��1��ʹ��ͭ˿���ŵ��� ��
��2��װ��A�з�Ӧ����ʽΪ ��
װ��C ��ʢ�ŵ�ҩƷ�� ��������ĸ���ţ�
A��Ũ���� B��NaOH ��Һ C��ˮ D�����Ȼ�̼
����F������ ��
��3����С���ȡ5.000g��ȡ����Ʒ����ˮ���250.0 mL��Һ��ȡ25.00mL��Һ����ƿ�У���0.1000mol/L����KMnO4��Һ���еζ���ʵ�������������±���ʾ��
����� | 1 | 2 | 3 | 4 |
����KMnO4��Һ���/mL | 20.70 | 20.12 | 20.00 | 19.88 |
�� ��һ��ʵ�����ݳ����쳣����������쳣��ԭ������� ������ĸ���ţ���
A����ƿϴ����δ����
B����ʽ�ζ���������ˮϴ����δ�ñ�Һ��ϴ
C���ζ��յ�ʱ���Ӷ���
������KMnO4��Һ�ζ�����������Һ�����ӷ���ʽΪ ��
������Ʒ���������Ƶ���������Ϊ ��