题目内容
7.有a、b、c、d四种金属.将a与b用导线连接起来,浸入电解质溶液中,外电路电流从b流向a.将a、d分别投入等浓度盐酸中,d比a反应剧烈.将铜浸入b的盐溶液里,无明显变化.如果把铜浸入c的盐溶液里,有金属c析出.据此判断它们的活动性由强到弱的顺序是( )| A. | dcab | B. | dabc | C. | dbac | D. | badc |
分析 原电池中被腐蚀的金属是活动性强的金属;金属和相同的酸反应时,活动性强的金属反应剧烈;金属的置换反应中,较活泼金属能置换出较不活泼的金属.
解答 解:两种活动性不同的金属和电解质溶液构成原电池,较活泼的金属作负极,负极上金属失电子发生氧化反应被腐蚀,较不活泼的金属作正极,电流由正极流向负极,所以a的活动性大于b;
金属和相同的酸反应时,活动性强的金属反应剧烈,将a、d分别投入等浓度盐酸溶液中,d比a反应剧烈,所以d的活动性大于a;
金属的置换反应中,较活泼金属能置换出较不活泼的金属,将铜浸入b的盐溶液中,无明显变化,说明b的活动性大于铜.如果把铜浸入c的盐溶液中,有金属c析出,说明铜的活动性大于c.
所以金属的活动性顺序为:d>a>b>c,故选B.
点评 本题考查了金属活动性强弱的判断,难度不大,能从原电池的负极、金属之间的置换反应、金属与酸或水反应的剧烈程度、金属氧化物的水化物的碱性强弱等方面来判断金属的活动性强弱.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
17.1mol某烃最多能和2molHCl发生加成反应,生成1mol氯代烷,1mol此氯代烷能和8molCl2发生取代反应,生成只含碳元素和氯元素的氯代烷,该烃可能是( )
| A. | CH3CH=CH2 | B. | CH2=CHCH=CH2 | C. | CH3=CHCH3 | D. | CH3-C≡CH2-CH3 |
18.下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
(1)在这10种元素中,非金属性最强的元素是Mg(填“元素符号”),金属性最强的元素是F(填“元素符号”),化学性质最不活泼的元素是Ar(填“元素符号”).
(2)元素①与②中,原子半径较大的是C(填“元素符号”).
(3)元素②与⑦形成的气态氢化物分别是:H2O和H2S(填化学式),两者的热稳定性大小为:前者>后者.(填“>”或“<”).
(4)元素④与⑤的最高价氧化物的水化物的碱性大小为:前者>后者.(填“>”或“<”).
(5)元素⑤的氧化物与盐酸反应的离子方程式为:Al2O3+6H+=2Al3++3H2O.
(6)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+H2O=2NaAlO2+3H2↑.
(7)元素④和⑧形成的化合物的类型(填离子化合物或共价化合物):离子化合物.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ⑩ | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)元素①与②中,原子半径较大的是C(填“元素符号”).
(3)元素②与⑦形成的气态氢化物分别是:H2O和H2S(填化学式),两者的热稳定性大小为:前者>后者.(填“>”或“<”).
(4)元素④与⑤的最高价氧化物的水化物的碱性大小为:前者>后者.(填“>”或“<”).
(5)元素⑤的氧化物与盐酸反应的离子方程式为:Al2O3+6H+=2Al3++3H2O.
(6)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+H2O=2NaAlO2+3H2↑.
(7)元素④和⑧形成的化合物的类型(填离子化合物或共价化合物):离子化合物.
15.下列变化,需要加入适当的氧化剂才能完成的是( )
| A. | PCl3→PCl5 | B. | MnO4-→Mn2+ | C. | SO2→SO32- | D. | FeCl3→FeCl2 |
2.卤代烃RCH2CH2X分子中的化学键如图所示,则下列说法正确的是 ( )
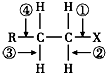

| A. | 当该卤代烃发生水解反应时,被破坏的键是①和③ | |
| B. | 当该卤代烃发生水解反应时,被破坏的键是① | |
| C. | 当该卤代烃发生消去反应时,被破坏的键是①和④ | |
| D. | 当该卤代烃发生消去反应时,被破坏的键是①和③ |
3.下列化学用语中,书写或说法正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 丙烷的球棍模型为 | |
| C. | 乙醇含有的官能团是-OH,带一个单位负电荷 | |
| D. | 乙酸的分子式为C2H4O2,其中CH3-在溶液中能电离出H+ |
4.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)画出元素④的原子结构示意图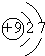 ,⑦元素的名称是硅,⑨元素的离子的电子式是
,⑦元素的名称是硅,⑨元素的离子的电子式是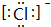 ,②的最简单气态氢化物中的化学键有极性键(填“离子键”、“极性键”或“非极性键”).
,②的最简单气态氢化物中的化学键有极性键(填“离子键”、“极性键”或“非极性键”).
(2)在标号元素中,最活泼的金属元素是(写元素符号)Na.最活泼的非金属元素是(写元素符号)F.
(3)⑦、⑧、⑨元素所形成的气态氢化物中,最稳定的是(写化学式)HCl.
(4)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是(写元素符号)Na>Al>Si.
(5)①与③形成共价化合物的电子式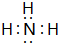 .用电子式表示⑤与⑧形成化合物的形成过程
.用电子式表示⑤与⑧形成化合物的形成过程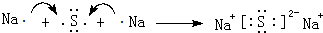 .
.
(6)⑦、⑧、⑨三种元素的最高价含氧酸的酸性由强到弱的顺序是(写化学式)HClO4>H2SO4>H2SiO3.
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
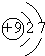 ,⑦元素的名称是硅,⑨元素的离子的电子式是
,⑦元素的名称是硅,⑨元素的离子的电子式是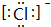 ,②的最简单气态氢化物中的化学键有极性键(填“离子键”、“极性键”或“非极性键”).
,②的最简单气态氢化物中的化学键有极性键(填“离子键”、“极性键”或“非极性键”).(2)在标号元素中,最活泼的金属元素是(写元素符号)Na.最活泼的非金属元素是(写元素符号)F.
(3)⑦、⑧、⑨元素所形成的气态氢化物中,最稳定的是(写化学式)HCl.
(4)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是(写元素符号)Na>Al>Si.
(5)①与③形成共价化合物的电子式
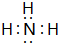 .用电子式表示⑤与⑧形成化合物的形成过程
.用电子式表示⑤与⑧形成化合物的形成过程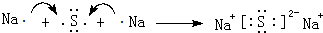 .
.(6)⑦、⑧、⑨三种元素的最高价含氧酸的酸性由强到弱的顺序是(写化学式)HClO4>H2SO4>H2SiO3.
 将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见氧化物,气体E是单质F所含元素的氢化物.
将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见氧化物,气体E是单质F所含元素的氢化物.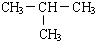 ;
;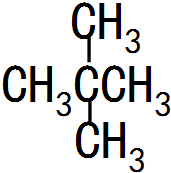 (写结构简式),它的一氯代物有1种.
(写结构简式),它的一氯代物有1种.