题目内容
【题目】某溶液中含如下离子组中的几种![]()
![]()
![]()
![]() ,某同学欲探究该溶液的组成进行了如下实验:
,某同学欲探究该溶液的组成进行了如下实验:
Ⅰ.用铂丝醮取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,此时溶液颜色加深,但无沉淀生成
Ⅲ.取Ⅱ反应后溶液分别置于两支试管中,第一支试管中加入 BaCl2 溶液有白色沉淀生成, 再滴加 KSCN 溶液,上层清液变红,第二支试管加入 CCl4,充分振荡静置后溶液分层,下层为无色。
下列说法正确的是( )
A.原溶液中肯定不含 ![]()
B.原溶液中肯定含有 ![]()
C.步骤Ⅱ中无色气体是 NO 气体,无 CO2 气体产生
D.为确定是否含有 Cl-可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀
【答案】C
【解析】
根据实验Ⅰ的焰色反应证明含有K+,实验Ⅲ检测出经过实验Ⅱ后溶液含有Fe3+,证明原溶液一定不含CO32-,根据实验Ⅱ加入盐酸,无沉淀说明不含SiO32-,有无色气体产生只能是![]() (H+)被还原生成一氧化氮气体,证明含有硝酸根离子,且此时溶液颜色加深,还原剂可能为Fe2+或
(H+)被还原生成一氧化氮气体,证明含有硝酸根离子,且此时溶液颜色加深,还原剂可能为Fe2+或![]() ,实验Ⅲ加入CCl4,充分振荡静置后溶液分层,下层为无色,证明不含碘单质,从而证明原溶液不含
,实验Ⅲ加入CCl4,充分振荡静置后溶液分层,下层为无色,证明不含碘单质,从而证明原溶液不含![]() 含有Fe2+,实验Ⅲ加入BaCl2 溶液有白色沉淀生成,证明含有
含有Fe2+,实验Ⅲ加入BaCl2 溶液有白色沉淀生成,证明含有![]() ,Fe3+和Cl-是否存在无法确定。
,Fe3+和Cl-是否存在无法确定。
A.根据分析,原溶液中一定含有![]() 和Fe2+,A项错误;
和Fe2+,A项错误;
B.根据分析,原溶液中Fe3+ -是否存在无法确定,B项错误;
C.根据分析,步骤Ⅱ中无色气体是NO气体,无CO2气体产生,C项正确;
D.使用硝酸银溶液检测是否含有 Cl-,硫酸根离子会干扰,D项错误;
答案选C。

【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易反应,生成一种氯化物和两种氧化物。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:
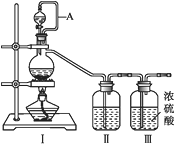
为制备纯净干燥的气体,下表中缺少的药品是:
装置Ⅰ | 装置Ⅱ | ||
烧瓶中 | 分液漏斗中 | ||
制备纯净Cl2 | MnO2 | ① | ② |
制备纯净NO | Cu | ③ | ④ |
②___________,③___________。
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→___________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅶ的作用为________________,若无该装置,Ⅸ中NOCl可能发生反应的化学方程式为_______________________________。
③乙组同学认为氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,所以装置Ⅷ不能有效除去有毒气体。为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是__________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为___________________。
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度
取Ⅸ中所得液体mg溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4溶液为指示剂,用c mol/LAgNO3 标准溶液滴定至终点,消耗标准溶液的体积为b mL。(已知:Ag2CrO4为砖红色固体)
①亚硝酰氯(NOCl)的质量分数为_________(用代数式表示即可)。
②若滴定前,滴定管尖嘴有气泡,滴定后气泡消失,则所测亚硝酰氯的纯度_________(偏高、偏低、无影响)
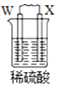
【题目】由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
甲 | 乙 | 丙 | |
装置 |
|
|
|
现象 | 金属W不断溶解 | Y 的质量增加 | W上有气体产生 |
A.四种金属的活动性强弱顺序为Z>W>Y>X
B.装置乙中Y电极上的反应式为Cu2++2e=Cu
C.装置甲中X作原电池正极
D.装置丙中溶液的c(H+)减小
【题目】重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。
Ⅰ.某工业废水中主要含有Cr3+,同时还含有少量的Fe2+、Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:
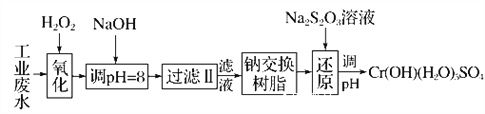
注:常温下,部分阳离子以氢氧化物形式完全沉淀时所需的pH,如下表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 9.6 | 11.1 | 8 | 9 |
(1)氧化过程中可代替H2O2加入的试剂是________(填字母,下同)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________;
已知钠离子交换树脂的原理:Mn++nNaR―→MRn+nNa+,此步操作被交换除去的杂质离子是____________。
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
(3)还原过程在酸性条件下进行,每消耗0.8 mol Cr2O![]() 转移4.8 mol e-,该反应离子方程式为________________________________________________________________________。
转移4.8 mol e-,该反应离子方程式为________________________________________________________________________。
Ⅱ.酸性条件下,六价铬主要以Cr2O![]() 形式存在,工业上常用电解法处理含Cr2O
形式存在,工业上常用电解法处理含Cr2O![]() 的废水,该法用Fe作电极电解含Cr2O
的废水,该法用Fe作电极电解含Cr2O![]() 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液。
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液。
(1)电解时能否用Cu电极来代替Fe电极?________(填“能”或“不能”),理由是_____________。
(2)常温下,Cr(OH)3的溶度积Ksp=1×10-20,假设溶液的c(Cr3+)=0.01mol/L,当pH应为______时开始生成沉淀。