��Ŀ����
����Ŀ��ij�о���ѧϰС��̽��FeSO4�Ļ�ѧ���ʺ���;���ش��������⣺
��1��̽��FeSO4��Һ������ԣ�ȡ����FeSO4���壬����ʯ����Һ����FeSO4��Һ������ԣ�����ѡ�õ������н�ͷ�ιܡ�ҩ�� ��
A�������� B���Թ� C����ƽ D����Ͳ
��2��������ͼװ��̽��FeSO4���ȶ���
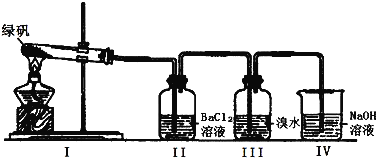
��II���а�ɫ�������ɣ�С���Ա������۷�������Ϊ���зֽ���ﲻ���ܵ��� ��
A��Fe2O3 ��SO3 ��H2O
B��Fe2O3 ��SO2 ��SO3 ��H2O
C��FeO ��Fe2O3 ��SO2 ��SO3 ��H2O
��III����ˮ�����������Ƿ���SO2�������ɣ�����SO2���ɣ���ˮ����ɫ��ʵ���У��۲쵽��ˮ��ɫ���ݴ��Ʋ�FeSO4�ֽ����п��ܱ�������Ԫ���� ��
��NaOH������������SO2���壬��д�����������SO2����ķ�Ӧ��ѧ����ʽ�� ��
��3��̽��FeSO4��Fe2+��ԭ�ԣ�
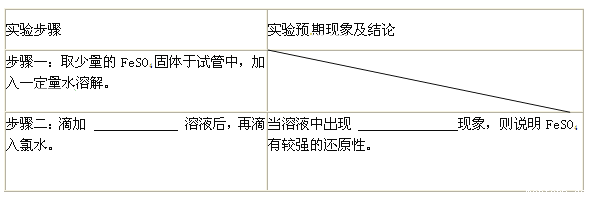
֤��FeSO4�н�ǿ�Ļ�ԭ�ԣ�����±���
��4������������;̽��
ȱ����ƶѪ�����ڷ������������������������Ƴ�ҩƬʱ���������һ����������£��������� ��
���𰸡�
��1��B��
��2����A����Fe����NaOH+SO2=NaHSO3��
��3��KSCN���������Ա仯��������
��4����ֹFeSO4������
��������
�����������1��ȡҩ��ȡ����Na2S2O3�������Թ����ܽ⣬�ý�ͷ�ιܵ���ʯ����Һ�ⶨNa2S2O3��Һ������ԣ�����ѡ�õ������н�ͷ�ιܡ�ҩ�ס��Թܣ��ʴ�Ϊ��B��
��2��������������ԭ��Ӧ���������ϼ��������н���A��Fe2O3��SO3��H2O���ϼ�ֻ���������ˣ�û�н��͵ģ���A�����ܣ� B��Fe2O3��SO2��SO3��H2O���������ˣ���B���ܣ�C��FeO��Fe2O3��SO2��SO3��H2O���������ˣ���C���ܣ���ѡ��A��
��FeSO4���������Ӿ��л�ԭ�ԣ��������п��ܱ�������Ԫ����Fe���ʴ�Ϊ��Fe��
����������������������Ʒ�Ӧ������������������Ӧ����ʽΪNaOH + SO2 = NaHSO3���ʴ�Ϊ��NaOH + SO2 = NaHSO3��
��3��FeSO4�н�ǿ�Ļ�ԭ�ԣ������ױ�����������Ϊ�������������������Ժ���������ӵĴ��ڼ��ɣ������ǣ�ȡ������FeSO4�������Թ��У�����һ����ˮ�ܽ⣬�������������軯����Һ�ټ�����ˮ�������Һ���ɫ������֤������������ǿ��ԭ�ԣ��ʴ�Ϊ��KSCN���������Ա仯��������
��4�����������������ױ������е�����������ȱ����ƶѪ�����ڷ������������������������Ƴ�ҩƬʱ���������һ����������£��������Ƿ�ֹ�����������������ʴ�Ϊ����ֹ����������������




