题目内容
【题目】某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
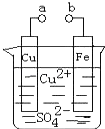
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e﹣=Cu
C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成 浅绿色
D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
【答案】D
【解析】
试题分析:a和b不连接时,铁与硫酸铜反应生成硫酸亚铁和铜,铁片上会有金属铜析出,故A正确;a和b用导线连接时构成原电池,铁是负极,铜是正极,铜片上发生的反应为:Cu2++2e﹣=Cu,故B正确;无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成 浅绿色,故C正确;a和b分别连接直流电源正、负极构成电解池,铜是阴极,电压足够大时,Cu2+向铁电极移动,故D错误。

练习册系列答案
相关题目
【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系下表:
温度℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是( )
A. 上述生成Ni(CO)4(g)的反应为放热反应
B. 25℃时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10-5
C. 80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2mol/L
D. 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)>v(逆)