题目内容
【题目】Ⅰ、在水的电离平衡中,c(H+)和 c(OH-)的关系如图所示:
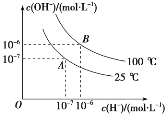
(1)100 ℃时,若向水中滴加盐酸,___(填“能”或“不能”)使体系处于 B 点状态。
(2)25 ℃时,将 pH=9 的 NaOH 溶液与 pH=4 的硫酸溶液混合,所得混合溶液的 pH=7,则 NaOH 溶液与硫酸溶液的体积比为___。
(3)100 ℃时,若盐酸中c(H+)=5×10-5 mol·L-1,则由水电离产生的 c(H+)=____。
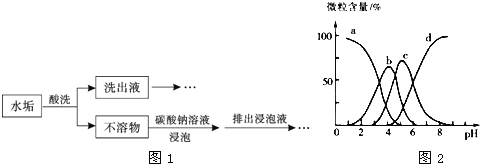
Ⅱ、已知在 25 ℃时,醋酸、次氯酸、碳酸和亚硫酸的电离平衡常数分别为醋酸K=1.75×10-5,次氯酸 K=2.95×10-8,碳酸 K1=4.30×10-7 ,K2=5.61×10-11,亚硫酸K1=1.54×10-2,K2=1.02×10-7
(4)写出碳酸的第一级电离平衡常数表达式K1=___。
(5)在相同条件下,等浓度的 CH3COONa、NaClO、Na2CO3、NaHCO3、Na2SO3 和 NaHSO3 溶液中碱性最强的是_____。等浓度的 Na2CO3 和 NaHCO3 的混合溶液中各离子浓度大小顺序为______。
(6)若保持温度不变,在醋酸溶液中通入少量 HCl(g),下列量会变小的是_____(填字母序号,下同)。
a.c(CH3COO-) b.c(H+) c.醋酸的电离平衡常数 d.c(CH3COOH)
(7)下列离子方程式中错误的是_____。
a 少量 CO2 通入次氯酸钠溶液中:CO2+H2O+ClO-=HCO![]() +HClO
+HClO
b 少量 SO2 通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
c 过量 CO2 通入澄清石灰水中:CO2+OH-=HCO![]()
【答案】不能 10:1 2×10-8 mol·L-1 ![]() Na2CO3 c(Na+)>c(
Na2CO3 c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+) a b
)>c(OH-)>c(H+) a b
【解析】
I.(1)酸、碱的电离抑制水的电离,据此分析;
(2)25 ℃时,pH=7的溶液显中性,酸碱恰好完全反应;
(3)酸溶液中氢氧根全部由水电离;
II.(5)酸的电离平衡常数越大,同浓度下酸性越强,相应的同浓度的强碱弱酸盐的碱性就越强;
(6)HCl可以电离出氢离子,使醋酸的电离平衡逆向移动;
(7)根据强酸制弱酸判断。
(1)向溶液中滴加盐酸会对水的电离起到抑制作用,氢离子浓度增大,氢氧根浓度减小,但是温度不变,水的离子积不变,所以不会处于B点位置,应沿曲线向右下方移动;
(2)pH=9 的 NaOH 溶液中c(OH-)=10-5mol/L,pH=4的硫酸溶液中c(H+)=104mol/L;设NaOH溶液的体积为V1,硫酸的体积为V2,混合后溶液pH=7,所以10-5mol/L×V1=104mol/L×V2,解得V1:V2=10:1;
(3)盐酸中c(H+)=5×10-5mol·L-1,据图可知100℃时水溶液中c(H+)·c(OH-)=10-12,所以此时溶液中c(OH-)=![]() =2×10-8mol·L-1,,水电离产生的氢氧根和氢离子浓度相等,所以由水电离产生的 c(H+)=2×10-8mol·L-1;
=2×10-8mol·L-1,,水电离产生的氢氧根和氢离子浓度相等,所以由水电离产生的 c(H+)=2×10-8mol·L-1;
(4)碳酸的第一步电离方程式为H2CO3![]()
![]() +H+,所以Ka1=
+H+,所以Ka1=![]() ;
;
(5)根据各酸的电离平衡常数可知酸性最弱的为![]() ,所以碱性最强的是Na2CO3;等浓度的Na2CO3和NaHCO3的混合溶液显碱性,所以(OH-)>c(H+),碳酸根的水解程度大于碳酸氢根,所以c(
,所以碱性最强的是Na2CO3;等浓度的Na2CO3和NaHCO3的混合溶液显碱性,所以(OH-)>c(H+),碳酸根的水解程度大于碳酸氢根,所以c(![]() )>c(
)>c(![]() ),所以混合溶液中c(Na+)>c(
),所以混合溶液中c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+);
)>c(OH-)>c(H+);
(6)a.HCl会电离出氢离子,使醋酸的电离平衡逆向移动,醋酸根浓度减小,故a符合题意;
b.HCl会电离出氢离子,所以溶液中氢离子浓度增大,故b不符合题意;
c.温度不变醋酸的电离平衡常数不变,故c不符合题意;
d.醋酸的电离平衡逆向移动,醋酸的浓度增大,故d不符合题意;
综上所述选a;
(7)a.根据电离平衡常数可知酸性:碳酸>次氯酸>碳酸氢根,所以即便少量二氧化碳通入次氯酸钠溶液中也无法生成碳酸根,离子方程式为CO2+H2O+ClO-=HCO![]() +HClO,a正确;
+HClO,a正确;
b.次氯酸根具有氧化性,会将二氧化硫氧化成硫酸根,所以离子方程式为Ca2++ClO-+SO2+H2O=CaSO4↓+2H++Cl-,b错误;
c.过量CO2通入澄清石灰水中,二氧化碳会和碳酸根、水反应生成碳酸氢根,碳酸氢钙可溶于水,所以离子方程式为CO2+OH-=HCO![]() ,c正确;
,c正确;
综上所述答案为b。

【题目】Ⅰ.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:①CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1;②CO(g)+2H2(g)
CH3OH(g)+H2O(g) △H1;②CO(g)+2H2(g)![]() CH3OH(g) △H2 ③CO2(g)+H2(g)
CH3OH(g) △H2 ③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3;
CO(g)+H2O(g) △H3;
化学键 | H-H | C-O | C | H-O | C-H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | X |
回答下列问题:
(1)已知△H2=-99 kJ·mol-1,则根据上表相关的化学键键能(“C![]() O”表示CO的化学键)计算X=_______ kJ·mol-1。
O”表示CO的化学键)计算X=_______ kJ·mol-1。
(2)反应①、②、③对应的平衡常数K1、K2、K3之间的关系式为___________。
(3)根据化学反应原理,分析增大压强对反应③的影响为_______________。(提示:从对反应速率、平衡状态、转化率角度回答)
Ⅱ.清洁能源具有广阔的开发和应用前景,可减小污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池。一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)![]() CH3OH(g)△H=-99kJmol-1。向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:
CH3OH(g)△H=-99kJmol-1。向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:
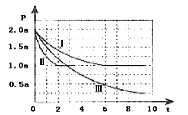
①Ⅱ和Ⅰ相比,改变的反应条件是_________;
②反应Ⅰ在6min时到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)=_________;
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=_________;
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1_____T3(填“>”“<”“=”),判断的理由是_________。
【题目】过碳酸钠(2Na2CO33H2O2)俗称固体双氧水。实验室可用碳酸钠和双氧水等为原料来制备,具体流程如下:

已知:①相关反应的方程式如下:2Na2CO3+3H2O2=2Na2CO33H2O2△H<0
②工业上常以产品活性氧的质量分数[ω(活性氧)=![]() ×100%]来衡量产品的优劣,13.00%以上为优等品。
×100%]来衡量产品的优劣,13.00%以上为优等品。
请回答:
表1 反应温度对产品收率及活性氧含量的影响
反应温度/℃ | 产品收率/% | 活性氧质量分数/% |
5 | 65.3 | 12.71 |
10 | 73.2 | 13.24 |
15 | 85.0 | 13.55 |
20 | 83.2 | 13.30 |
25 | 55.1 | 12.78 |
表2加料时间对产品收率及活性氧含量的影响
加料时间/min | 产品收率/% | 活性氧质量分数/% |
5 | 65.7 | 13.30 |
10 | 76.8 | 14.75 |
15 | 81.3 | 14.26 |
20 | 89.0 | 13.82 |
25 | 87.9 | 13.51 |
(1)分析表1,一般选择的反应温度为_____。
(2)分析表2,加料时间对产品收率也有很大影响,时间太短或太长均不利于生产,加料时间太短导致产品收率较低的原因是_____。
(3)结晶过程中加入氯化钠,作用是_____。
(4)下列关于抽滤操作,正确的是_____。
A.准备略大于漏斗内径的滤纸,以盖住布氏漏斗瓷板上的小孔
B.用倾析法先转移溶液,待溶液快流尽时再转移沉淀
C.洗涤沉淀时,加入少量水并开大水龙头,重复操作2~3次
D.用玻璃棒轻轻刮下抽滤得到的固体,晾干后保存在试剂瓶中
(5)使用图2所示装置抽滤,中途需停止抽滤时,最佳操作为_____。
(6)产品出厂前需测定活性氧的质量分数,现将0.1000g某厂的产品(所含杂质均不参与反应)溶于水配成溶液,加入10.00mL1.000molL﹣1的稀硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量_____,用0.1000molL﹣1的Na2S2O3标准溶液滴定,若该产品的活性氧质量分数为13.60%,则达到滴定终点时共消耗标准液的体积为_____mL。[已知:2Na2S2O3+I2=Na2S4O6+2NaI]