题目内容
15.下列说法正确的是( )| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | 漂白粉的有效成分为CaCl2和Ca(ClO)2 | |
| C. | 实验室制备Cl2,可用向上排空气法或排饱和食盐水法收集 | |
| D. | 新制氯水只含有氯气和次氯酸分子 |
分析 A、氯气在化学反应中既可以做氧化剂,还可以做还原剂;
B、漂白粉的有效成分为Ca(ClO)2;
C、食盐水溶液中的氯离子抑制氯气的溶解,可以用排饱和食盐水法收集氯气,氯气密度大于空气,所以也可用向上排空气法收集;
D、新制氯水含有水、氯气和次氯酸分子.
解答 解:A、氯气在和水以及强碱的反应中既做氧化剂,还做还原剂,故A错误;
B、漂白粉的有效成分为Ca(ClO)2,故B错误;
C、氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和食盐水除去氯气中混有的氯化氢气体,又氯气密度大于空气,所以也可用向上排空气法收集,故C正确;
D、新制氯水含有水、氯气和次氯酸分子,故D错误.
故选C.
点评 本题涉及氯气的性质、漂白粉的有效成分、氯气的收集方法等知识的掌握,难度不大.

练习册系列答案
相关题目
5.下列物质属于新型无机非金属材料的是( )
| A. | 水泥 | B. | 光导纤维 | C. | 玻璃 | D. | 陶瓷 |
6.苹果酸的结构简式为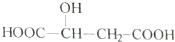 ,下列说法中不正确的是( )
,下列说法中不正确的是( )
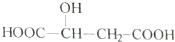 ,下列说法中不正确的是( )
,下列说法中不正确的是( )| A. | 苹果酸中能发生酯化反应的官能团有2种 | |
| B. | 1mol苹果酸可与2molNaOH发生中和反应 | |
| C. | 苹果酸可以发生消去反应,生成的有机物存在顺反异构体 | |
| D. |  与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
10.下列各组液体混合物,用分液漏斗能分开的是( )
| A. | 苯和硝基苯 | B. | 液溴和四氯化碳 | C. | 乙醛和水 | D. | 溴苯和水 |
20.下列各组溶液中,c(NO3-)物质的量浓度最大的是( )
| A. | 500mL 1mol/L K NO3 | B. | 800mL 0.5mol/L Mg (NO3)2 | ||
| C. | 250mL 1mol/LFe(NO3)3 | D. | 200mL 1mol/L Ca(NO3)2 |
7.如果a克氨气由b个原子构成,则在2a克硫化氢中含有的分子数为( )
| A. | 0.25b | B. | 0.5b | C. | 2b | D. | 4b |
4.下列材料的特性及用途叙述不正确的是( )
| A. | 氧化铝陶瓷具有两性,可用来制造人造牙齿 | |
| B. | 氮化硅陶瓷耐高温且不易传热,可用来制造柴油机 | |
| C. | 光导纤维传导光的性能很强,是非常好的通讯材料 | |
| D. | 人造刚玉硬度高,用于制造刚玉球磨机 |
5.某同学在实验室中进行如下实验:
以下结论不正确的是( )
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 |  |  | 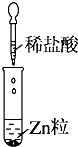 |
| 现象 | 没有明显变化,溶液仍为无色 | 有沉淀生成,溶液为蓝色 | 有无色气体放出 |
| A. | Ⅰ中无明显变化,说明两溶液不反应 | |
| B. | Ⅱ中的白色沉淀为BaSO4 | |
| C. | Ⅲ中的离子方程式为2H++Zn═Zn2++H2↑ | |
| D. | Ⅲ中发生的反应也是氧化还原反应 |