题目内容
18.下列图示的化学实验操作中,正确的是( )| A. | 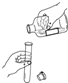 倾倒液体 | B. |  取粉末状固体药品 | ||
| C. | 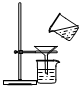 过滤 | D. |  浓硫酸的稀释 |
分析 A.倾倒液体时注意:瓶口、标签的位置、瓶塞的放置等;
B.取用粉末状药品:一横、二放、三慢竖;
C.过滤实验时要“一贴二低三靠”;
D.稀释浓硫酸时,将浓硫酸沿容器壁慢慢注入水中.
解答 解:A.倾倒液体时,瓶口与试管口紧挨,防止药品流出;标签朝向手心,防止流出的药品污染标签;瓶塞倒放,防止污染瓶塞、从而污染药品,故A错误;
B.取用固体粉末状药品时,试管横放,将药品用纸槽或药匙送入试管底部,再慢慢竖起试管,故B正确;
C.过滤时液体要用玻璃棒引流,漏斗的下端口紧挨接受的烧杯内壁,故C错误;
D.稀释浓硫酸时,将浓硫酸沿容器壁慢慢注入水中,并不断搅拌,故D错误.
故选B.
点评 本题考查实验基本操作,有倾倒液体、取用固体、过滤实验、稀释浓硫酸,都是常用到的基础知识,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
8.下列铁的化合物可以分别通过化合反应、置换反应、复分解反应生成的是( )
| A. | FeCl2 | B. | Fe3O4 | C. | Fe(OH)3 | D. | Fe2(SO4)3 |
9.如图是关于N2+3H2?2NH3(正反应为放热反应)的速率一时问图象,则t1时刻使平衡发生移动的原因是( )

| A. | 升高温度,同时增大压强 | |
| B. | 降低温度.同时减小压强 | |
| C. | 增大反应物的浓度,同时使用适宜的催化剂 | |
| D. | 增大反应物的浓度,同时减小生成物的浓度 |
6.一定条件下,在体积为10L的固定容器中发生的反应:N2+3H2?2NH3,反应过程如图所示,下列说法正确的是( )

| A. | t1min时正、逆反应速率相等 | |
| B. | X曲线表示NH3的物质的量随时间变化的关系 | |
| C. | 0~8 min,H2的平均反应速率v(H2)=0.75 mol•L-1•min-1 | |
| D. | 10~12 min,N2的平均反应速率为v(N2)=0.25mol•L-1•min-1 |
3.有四种物质的溶液:①Ba(OH)2、②Na2SO4、③HNO3、④CuCl2,不用其他试剂就可将它们逐一鉴别出来,其鉴别顺序是( )
| A. | ④①②③ | B. | ①③④② | C. | ④③②① | D. | ①④②③ |
10.下列有关实验数据处理,正确的是( )
| A. | 用pH试纸测得新制氯水的pH为2 | |
| B. | 中和滴定实验中,滴定管内液面对应的刻度由0 mL变为10 mL | |
| C. | 某同学在托盘天平左盘放置5g砝码,游码位于0.5g处,则所得药品质量为5.5g | |
| D. | 质量分数为20%的NaCl溶液与水等质量混合,稀释后溶液的质量分数必为10% |
7.在一定条件下,NO跟NH3可以发生反应:6NO+4NH3=5N2+6H2O,关于该反应下列说法中不正确的是( )
| A. | H2O既不是氧化产物也不是还原产物 | |
| B. | 该反应中被氧化和被还原的氮元素的质量比是3:2 | |
| C. | 若有2mol NH3完全反应,共转移12mol电子 | |
| D. | NO是氧化剂,NH3是还原剂 |
20.下列四种溶液中:①pH值为0的盐酸;②0.1mol/L的盐酸;③0.01mol/L的氢氧化钠溶液;④pH为11的氢氧化钠溶液.由水电离生成的c(H+)之比依次为( )
| A. | 0:1:12:11 | B. | 14:13:12:11 | C. | 14:13:2:3 | D. | 1:10:100:1000 |