题目内容
13.下列有关铁、铝及其合金的说法正确的是( )| A. | 铁、铝的都属于轻金属 | |
| B. | 生铁的硬度和熔点都比纯铁高 | |
| C. | 铁、铝的单质都具有银白色金属光泽,都属于有色金属 | |
| D. | 金属形成合金后通常具有更多优良性能,所以用途更广泛 |
分析 A.一般指密度大于4.5g/cm3的金属叫重金属,包括铜、铅、锌、镍、钴、锡、汞等.一般把密度小于4.5g/cm3的金属叫轻金属,如钠、镁、铝、钙、锶、钡等;
B.合金的硬度大,熔点低;
C.铁、铬、锰及其合金属于黑色金属,其余金属属于有色金属;
D.合金的硬度大,熔点低,耐腐蚀.
解答 解:A.铁属于重金属,故A错误;
B.生铁的熔点都比纯铁低,故B错误;
C.铁属于黑色金属,故C错误;
D.合金的硬度大,熔点低,耐腐蚀,用途更广泛,故D正确.
故选D.
点评 本题考查金属的分类和性质,题目难度不大,注意重金属、轻金属、有色金属的区别,平时注意相关知识的积累.

练习册系列答案
相关题目
4.在CuCl2水溶液中存在如下平衡:
[Cu(H2O)4]2++4Cl-?[CuCl4]2-+4H2O
(蓝) (绿)
能使黄绿色CuCl2溶液向蓝色转化的操作是( )
[Cu(H2O)4]2++4Cl-?[CuCl4]2-+4H2O
(蓝) (绿)
能使黄绿色CuCl2溶液向蓝色转化的操作是( )
| A. | 蒸发浓缩 | B. | 加水稀释 | C. | 加入AgNO3 | D. | 加入食盐晶体 |
1.铁和下列物质反应,能生成+3价化合物的是( )
①O2 ②S ③HCl ④CuCl2 ⑤HNO3 ⑥溴 ⑦H2O.
①O2 ②S ③HCl ④CuCl2 ⑤HNO3 ⑥溴 ⑦H2O.
| A. | ①②⑤ | B. | ①⑥ | C. | ①⑤⑥⑦ | D. | ①⑤⑥ |
8.有四种微粒的结构示意图: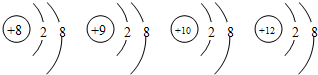 ,下列叙述中错误的是( )
,下列叙述中错误的是( )
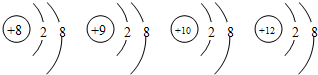 ,下列叙述中错误的是( )
,下列叙述中错误的是( )| A. | 它们属于不同元素 | |
| B. | 它们都是离子 | |
| C. | 它们的最外层都具有稀有气体原子的稳定结构 | |
| D. | 它们的核外电子排布均相同 |
2.在四种化合物①NaHCO3 ②Al(OH)3 ③葡萄糖 ④H2N-CH2-COOH中,跟盐酸和氢氧化钠溶液都能反应的是( )
| A. | 只有②③④ | B. | 只有①②④ | C. | 只有①② | D. | 有①②③④ |