题目内容
【题目】根据要求回答下列问题:
I. ①H、D、T ②H2O、D2O ③石墨、金刚石 ④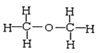 和
和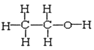 ⑤
⑤
四组微粒或物质中,互为同位素的是_______;(填序号,下同)互为同素异形体的是_____;互为同分异构体的是_____。
II.现有①金刚石 ②干冰 ③Na2SO4 ④NH4Cl 四种物质,按下列要求回答:
(1)晶体熔化时需要破坏共价键的是_____(填序号,下同);
(2)熔点最低的是_______;
(3)晶体中只存在一种微粒作用力是_______;
(4)属于离子晶体的是________。
【答案】① ③ ④ ① ② ① ③④
【解析】
I.同位素是质子数相同、中子数不同的原子互称同位素;
同素异形体是同种元素组成的不同性质的单质;
同分异构体是分子式相同结构不同的化合物;
II.原子晶体是由原子通过共价键结合而成;离子晶体是离子间通过离子键结合成;分子晶体构成微粒是分子通过分子间作用力结合而形成;微粒间作用力大小关系一般为原子晶体>离子晶体>金属晶体>分子晶体,据此分析解答。
I.①H、D、T是质子数相同、中子数不同的原子,三者互为同位素;
③石墨、金刚石是C元素构成的不同性质的单质,二者互为同素异形体;
④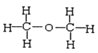 和
和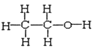 中前者是二甲醚,后者是乙醇,二者分子式都是C2H6O,结构不同,二甲醚和乙醇二者互为同分异构体;
中前者是二甲醚,后者是乙醇,二者分子式都是C2H6O,结构不同,二甲醚和乙醇二者互为同分异构体;
II.①金刚石是由C原子通过共价键结合而形成的空间网状结构的原子晶体,由于共价键结合力很强,断裂消耗很高能量,因此熔沸点高,硬度大;
②干冰是固体CO2,由CO2分子通过分子间作用力结合形成的分子晶体,分子间作用力很弱,因此熔沸点低,硬度小;
③Na2SO4是由Na+、SO42-通过离子键结合形成的离子晶体,在阴离子SO42-中存在共价键;离子键比共价键结合力弱,但比分子间作用力大很多;
④NH4Cl是由NH4+、Cl-通过离子键结合形成的离子晶体,在阳离子NH4+中存在共价键,晶体熔化断裂离子键。
综上所述可知(1)晶体熔化时需要破坏共价键的是①;
(2)熔点最低的是②;
(3)晶体中只存在一种微粒作用力是①;
(4) 属于离子晶体的是③④。

 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案