题目内容
【题目】实验室利用下图装置制备H2S气体,并探究H2S的有关性质。回答下列问题:
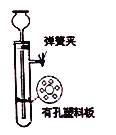
(1)实验开始时,检查装置气密性的方法是_________________。
(2)若装置不漏气,加入装置中的药品为_________(填字母)。
a.FeS和稀硫酸 b.Na2S和稀硫酸 C.ZnS和稀硝酸d.CuS和稀盐酸
该反应的离子方程式为_________________。
(3)打开弹簧夹使反应发生,将生成的H2S气体通入1.0mol/LFe(NO3)3溶液中,观察到有浅黄色固体析出。为探究实际参与该反应的微粒种类,设计如下图装置:

若A装置中加入1.0mol/L的FeCl3溶液,并测其pH=1,则B装置中加入的试剂是______;实验观察到A、B中均有浅黄色固体析出,则H2S与Fe(NO3)3溶液反应的离子方程式为_______。
(4)实验结束时,使反应停止的操作是______;此时反应停止的原因是______________。
(5)常温下,以Na2S为样品,选择合理的仪器和试剂设计实验①证明氢硫酸为二元弱酸②测量并估算氢硫酸的Ka2(H2S),则需要的主要计量仪器为电子天平、容量瓶、_____、_______。
【答案】 夹紧弹簧夹,往长颈漏斗中加水至漏斗管内液面高于试管内液面,一段时间后,液面差保持不变,证明气密性良好,否则气密性不好 a FeS + 2H+ = H2S↑+ Fe2+ 浓度分别为3.0 mol·L-1和0. 1mol·L-1的KNO3—HCl混合溶液 2H2S + Fe3+ + NO3- = 2S↓+Fe2+ + NO + 2H2O 用弹簧夹夹紧橡皮管 夹紧弹簧夹后,装置中产生的H2S难溶于稀硫酸,使试管内气体压强增大,将稀硫酸压回长颈漏斗使FeS固体和稀硫酸分离而停止反应 酸式滴定管 pH计
【解析】(1)检查装置的气密性原理通常是想办法造成装置不同部位有压强差,并产生某种明显现象,如气泡的生成,水柱生成,液面升降。对本装置检查气密性方法是:用弹簧夹夹紧橡皮管,往长颈漏斗中加水至漏斗管内液面高于试管内液面,一段时间后,液面差保持不变,证明气密性良好,否则气密性不好;
(2)制取硫化氢气体,FeS和稀硫酸反应生成硫化氢气体,且硫化亚铁不溶于水,a可以;Na2S和稀硫酸也能反应生成硫化氢气体,但硫化钠易溶于水,无法控制硫化氢气体产生的速度,所以b不符合实验装置要求;稀硝酸具有强氧化性,可以将-2价的硫氧化,不产生硫化氢气体,所以c不可以;CuS与稀盐酸不反应,所以d不可以,因此能够产生硫化氢气体且符合装置要求的是a;FeS和稀硫酸反应的离子方程式为:FeS+2H+=Fe2++H2S↑;
(3)H2S气体通入1.0mol/LFe(NO3)3溶液中,观察到有浅黄色固体析出,Fe3+与NO3-都能够与H2S反应产生S沉淀,Fe3+与NO3-有氧化性,A装置中加入1.0mol/L的FeCl3溶液,并使溶液的pH=1,确定是否是Fe3+引起的,因此B中应该验证是否是NO3-在酸性(PH=1)条件下引起的,B中可以加入浓度分别为3.0 mol·L-1和0. 1mol·L-1的KNO3—HCl混合溶液,即:B装置中加入的试剂是浓度分别为3.0 mol·L-1和0. 1mol·L-1的KNO3—HCl混合溶液;A、B中均有浅黄色固体析出,则H2S与Fe(NO3)3溶液反应的离子方程式为2H2S + Fe3+ + NO3- = 2S↓+Fe2+ + NO + 2H2O ;
(4)利用启普发生器制取气体的原理,关闭启普发生器的活塞,产生的气体将液体压回漏斗中,固体与液体分离,反应停止,所以本实验结束时,使反应停止的操作:用弹簧夹夹紧橡皮管;此时反应停止的原因是:夹紧弹簧夹后,装置中产生的H2S难溶于稀硫酸,使试管内气体压强增大,将稀硫酸压回长颈漏斗使FeS固体和稀硫酸分离而停止反应;
(5)用电子天平称取一定质量的Na2S样品,配制成0.001mol/L溶液,用PH计测定其溶液的PH,PH大于7,说明溶液呈碱性,证明Na2S发生水解反应,根据:S2-+H2O![]() HS-+OH-说明H2S是弱酸;再配制0.001mol/LH2SO4的稀溶液,取0.001mol/LNa2S溶液20.00ml于锥形瓶中,用0.001mol/LH2SO4溶液进行滴定,当滴入5ml0.001mol/L硫酸溶液时,此时溶液中S2-与HS-的浓度基本相同,用PH计测定溶液的PH,通过换算确定Ka2,Ka2=C(S2-)C(H+)/C(HS-)≈C(H+),因此,以Na2S为样品,选择合理的仪器和试剂设计实验①证明氢硫酸为二元弱酸②测量并估算氢硫酸的Ka2(H2S),则需要的主要计量仪器为电子天平、容量瓶、酸式滴定管和pH计,正确答案:酸式滴定管和pH计。
HS-+OH-说明H2S是弱酸;再配制0.001mol/LH2SO4的稀溶液,取0.001mol/LNa2S溶液20.00ml于锥形瓶中,用0.001mol/LH2SO4溶液进行滴定,当滴入5ml0.001mol/L硫酸溶液时,此时溶液中S2-与HS-的浓度基本相同,用PH计测定溶液的PH,通过换算确定Ka2,Ka2=C(S2-)C(H+)/C(HS-)≈C(H+),因此,以Na2S为样品,选择合理的仪器和试剂设计实验①证明氢硫酸为二元弱酸②测量并估算氢硫酸的Ka2(H2S),则需要的主要计量仪器为电子天平、容量瓶、酸式滴定管和pH计,正确答案:酸式滴定管和pH计。

【题目】苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
已知:

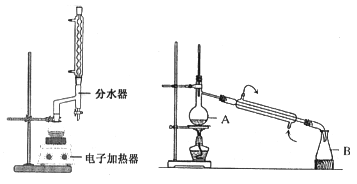
实验步骤如下:①在100 mL圆底烧瓶中加入12.20 g苯甲酸、25mL乙醇(过量)、20mL环己烷,以及4mL浓硫酸,混合均匀并加入沸石,按左上图所示装好仪器,控制温度在65~70℃加热回流2h。反应时环己烷-乙醇-水会形成“共沸物”(沸点62.6℃)蒸馏出来。再利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
④用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并有机层。加入氯化钙,对粗产品进行蒸馏(装置如图所示)。低温蒸出乙醚后继续升温,接收210~213℃的馏分。
⑤检验合格,测得产品体积为12.86mL.
(1)步骤①中使用分水器不断分离除去水的目的是_________________。
(2)步骤②中应控制馏分的温度在___________________。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(3)步骤③中若Na2CO3加入不足,在步骤④蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是_____________。
(4)步骤④中分液操作叙述正确的是__________。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞。将分液漏斗倒转用力振摇
B.振摇几次后需打开分液漏斗下口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.分液操作时,分液漏斗中的下层液体由下口放出,然后再将上层液体由下口放出
蒸馏装置图中仪器A的名称是___________,在步骤④中加入氯化钙的作用是_________。
(5)该实验产品的产率为____________。
【答案】 有利于平衡不断向正方向移动,提高苯甲酸乙酯产率 C 苯甲酸乙酯中混有苯甲酸,在受热至100℃时发生升华 AB 蒸馏烧瓶 吸水剂 90.02%
【解析】试题分析:本题考查苯甲酸乙酯的制备。
(1)反应![]() +CH3CH2OH
+CH3CH2OH![]()
![]() +H2O为可逆反应,使用分水器不断分离除去水,减小生成物浓度,有利于平衡不断向正反应方向移动,提高苯甲酸乙酯的产率。
+H2O为可逆反应,使用分水器不断分离除去水,减小生成物浓度,有利于平衡不断向正反应方向移动,提高苯甲酸乙酯的产率。
(2)根据题意,反应时环己烷-乙醇-水会形成“共沸物”蒸馏出来。烧瓶内的苯甲酸乙酯中混有乙醇、环己烷、苯甲酸和硫酸,步骤②继续加热蒸出苯甲酸乙酯中的乙醇、环己烷,乙醇的沸点为78.3℃,环己烷的沸点为80.8℃,苯甲酸乙酯的沸点为212.6℃,所以步骤②应控制馏分的温度在85~90℃,答案选C。
(3)步骤③中加入Na2CO3除去苯甲酸乙酯中混有的苯甲酸和硫酸,若Na2CO3加入不足,苯甲酸没有完全除去,步骤④蒸馏时蒸馏烧瓶中可见白烟的原因是:苯甲酸乙酯中混有苯甲酸,苯甲酸在受热至100℃时发生升华。
(4)A,为了使乙醚和水溶液充分接触,水溶液中加入乙醚转移至分液漏斗中后,需塞上玻璃塞,将分液漏斗倒转用力振摇,A项正确;B,为防止分液漏斗中气压过大将玻璃塞弹出,振摇几次后需打开分液漏斗下口的玻璃塞放气,B项正确;C,经几次振摇并放气后,需将分液漏斗置于铁架台上静置、待液体分层,C项错误;D,分液操作时,分液漏斗中的下层液体由下口放出,然后将上层液体从上口倾倒出来,D项错误;答案选AB。蒸馏装置图中仪器A的名称是蒸馏烧瓶。在步骤④中加入CaCl2的作用是作为吸水剂,除去水。
(5)由于乙醇过量,以苯甲酸计算理论生成的苯甲酸乙酯,![]() ~
~![]() ,n(苯甲酸乙酯)理论=n(苯甲酸)=
,n(苯甲酸乙酯)理论=n(苯甲酸)=![]() =0.1mol,m(苯甲酸乙酯)理论=0.1mol
=0.1mol,m(苯甲酸乙酯)理论=0.1mol![]() 150g/mol=15g,该实验产品的产率=
150g/mol=15g,该实验产品的产率=![]() 100%=90.02%。
100%=90.02%。
【题型】实验题
【结束】
19
【题目】根据下列四种元素的第一至第四电离能数据(单位:kJ/mol),回答下面各题:
元素代号 | I1 | I2 | I3 | I4 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
(1)在周期表中,最可能处于同一族的是___________
A.S和U B.S和T C.T和U D.R和T E.R和U
(2)T的氯化物的化学式为___________________
(3)如果U元素是短周期的元素,你估计它的第2次电离能飞跃数据将是第_____个。
(4)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是_________,其中元素_______的第一电离能反常高的原因是_____________。