题目内容
6.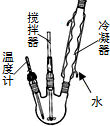 三乙酸甘油酯是一种优良的溶剂、定香剂和增塑剂.实验室制备三乙酸甘油酯的反应原理、实验装置及相关数据如下:3CH3COOH+
三乙酸甘油酯是一种优良的溶剂、定香剂和增塑剂.实验室制备三乙酸甘油酯的反应原理、实验装置及相关数据如下:3CH3COOH+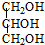 $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$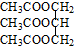 +3H2O
+3H2O| 物质 | 相对 分子质量 | 密度/g•cm-3 | 沸点/℃ | 水中 溶解性 |
| 甘油 | 92 | 1.2636 | 290 (分解) | 溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 三乙酸甘油酯 | 218 | 1.1596 | 258 | 不溶 |
步骤1.在500mL反应器中加入200g冰醋酸,92g甘油和100mL苯,开动搅拌器,慢慢从插温度计口加入3mL浓硫酸后,缓缓加热并回流1h,停止加热.
步骤2.用5%碳酸钠溶液洗涤,再用水洗涤,最后加入无水氯化钙.
步骤3.先进行常压蒸馏收集75~85℃馏分.
步骤4.将常压馏分再进行减压蒸馏,收集128~131℃/933Pa馏分,最终得产品176g.
(1)步骤1先开搅拌器后加浓硫酸的目的是防止局部浓硫酸浓度过大,造成有机物脱水炭化;冰醋酸过量的目的是有利于向酯化方向移动,提高甘油的转化率
(2)用5%碳酸钠溶液洗涤的主要目的是除去产品的硫酸、乙酸;加无水氯化钙的目的是除去有机物中的水份
(3)最后用减压蒸馏而不用常压蒸馏其原因是防止常压蒸馏温度过高导致产品分解
(4)本次实验产率为80.7%.
分析 本题以酯化反应的原理为载体,利用乙酸和甘油酯化得到三乙酸甘油酯的实验流程,主要考查的是结合浓硫酸的性质配制反应混合液,根据平衡理论通过增加冰醋酸的量提高甘油的利用率,反应后的混合物用饱和碳酸钠溶液洗涤除去催化作用的硫酸溶液和过量醋酸溶液,有氯化钙吸水干燥粗产品,最后采用减压蒸馏的方法得到产品,利用原子守恒可计算产率,据此解答;
(1)因浓硫酸有脱水性,搅拌可稀释均匀,避免产生炭化现象,利用平衡的理论,增大一种反应物的量可提高另一种反应物的转化率;
(2)反应后的混合液中存在催化作用的硫酸和过量的醋酸,可以用饱和碳酸钠溶液中和,氯化钙有吸水性,加入可除去混有的水;
(3)三乙酸甘油酯在高温下可能会分解,因此蒸馏时不能常压高温蒸馏;
(4)92g甘油的物质的量为$\frac{92g}{92g/mol}$=1mol,理论制得的三乙酸甘油酯也是1mol,可结合其质量计算产率.
解答 解:(1)浓硫酸有强氧化性,先开搅拌器后加浓硫酸可防止局部浓硫酸浓度过大,造成有机物脱水炭化;酯化反应可逆反应,增大乙酸的量,有利于向酯化方向移动,提高甘油的转化率,
故答案为:防止局部浓硫酸浓度过大,造成有机物脱水炭化;有利于向酯化方向移动,提高甘油的转化率;
(2)用5%碳酸钠溶液洗涤催化作用的硫酸和过量的乙酸,利用氯化钙的吸水性除去有机物中的水份,故答案为:除去产品的硫酸、乙酸; 除去有机物中的水份;
(3)为避免三乙酸甘油酯在高温下的分解,采用减压蒸馏,故答案为:防止常压蒸馏温度过高导致产品分解;
(4)1mol的甘油理论制得1mol的三乙酸甘油酯,质量为1mol×218g/mol=218g,产率为$\frac{176g}{218g}×100%$=80.7%,故答案为:80.7%.
点评 本题参照教材酯化反应的原理合成三乙酸甘油酯并涉及混合物的分离提纯,基础考查,难度不大,建议学生重视双基复习.

| A. | Na+、K+、CO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$ | B. | K+、Na+、NO${\;}_{3}^{-}$、CH3COO- | ||
| C. | Na+、K+、S2-、OH- | D. | H+、NH${\;}_{4}^{+}$、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$ |
| 容器 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 | |
| CO2 | H2S | H2O | |||
| Ⅰ | 607 | 0.11 | 0.41 | 0.01 | / |
| Ⅱ | 607 | 0.22 | 0.82 | / | |
| Ⅲ | 620 | 0.1 | 0.4 | / | 6.74×10-3 |
| A. | 该反应正反应为放热反应 | |
| B. | 607K时该反应的平衡常数为2.50×10-3 | |
| C. | 容器Ⅱ达到平衡时容器中COS的物质的量为0.02mol | |
| D. | 容器Ⅲ达平衡时,再充入少量氦气,平衡将向正反应方向移动 |
| A. | 升高温度,正反应速率增加,逆反应速率减小 | |
| B. | 升高温度有利于反应速率增加,从而缩短达到平衡的时间且提高A2的转化率 | |
| C. | 达到平衡后,同时升高温度和增大压强,有可能该平衡不发生移动 | |
| D. | 达到平衡后,降低温度或减小压强都有利于该平衡向正反应方向移动 |
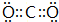 ;V原子的结构示意图
;V原子的结构示意图 ;Z的氢化物结构式为
;Z的氢化物结构式为 ;写出U元素在周期表中的位置第三周期VIA族;N2W2中含有的化学键有离子键、共价键(化学键类型)
;写出U元素在周期表中的位置第三周期VIA族;N2W2中含有的化学键有离子键、共价键(化学键类型)