��Ŀ����
����Ŀ��M�Ǻϳɿ����ػһ�ù�ص��м�����ϳ�·��������

��֪��
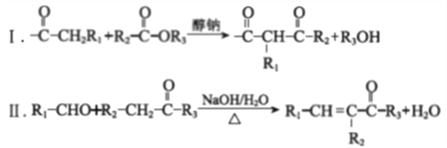
��R1��R2��R3������������ԭ����
��1��A�к��еĹ����ŵ�����Ϊ�Ѽ�����ԭ�ӡ�________��________��
��2��A��C��Ӧ�Ļ�ѧ����ʽ��________��
��3��C��D�ķ�Ӧ������________��
��4��E�Ľṹ��ʽ��________��
��5��I�ĺ˴Ź���������ֻ��һ�����շ���
������a��________��
��H��I��Ӧ�Ļ�ѧ����ʽ��________��
��I��K��Ӧ�Ļ�ѧ����ʽ��________��
��6��L�Ľṹ��ʽ��________��
���𰸡� �Ȼ� �ǻ�  ȡ����Ӧ
ȡ����Ӧ 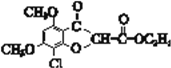 NaOHˮ��Һ������
NaOHˮ��Һ������ ![]()
![]()
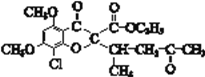
����������������������кϳ�·����Ϣ��֪��A���Ҵ�����������Ӧ����C��C��![]() ����ȡ����Ӧ����D��D�ڴ��Ƶ�����������E����EΪ
����ȡ����Ӧ����D��D�ڴ��Ƶ�����������E����EΪ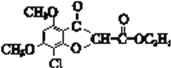 ��I�ĺ˴Ź���������ֻ��һ�����շ�����F�ķ���ʽ����ص�ת�����������ж�IΪ��ͪ������ϢII��֪��JΪ��ȩ��CH3CHO����KΪCH3CH=CHCOCH3�������ϢI��M��E��K�������ʵĽṹ�����Ƴ�LΪ
��I�ĺ˴Ź���������ֻ��һ�����շ�����F�ķ���ʽ����ص�ת�����������ж�IΪ��ͪ������ϢII��֪��JΪ��ȩ��CH3CHO����KΪCH3CH=CHCOCH3�������ϢI��M��E��K�������ʵĽṹ�����Ƴ�LΪ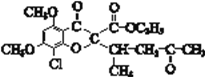 ��
��
��1��A�к��еĹ�����Ϊ�Ѽ�����ԭ�ӡ��Ȼ����ǻ���
��2��A��C��Ӧ�Ļ�ѧ����ʽ�� ��
��
��3��C��D�ķ�Ӧ������ȡ����Ӧ��
��4��E�Ľṹ��ʽ�� ��
��
��5����Ӧ����±����ˮ�ⷴӦ������a��NaOHˮ��Һ��������
��H��I��Ӧ�Ļ�ѧ����ʽ��![]() ��
��
��I��K��Ӧ�Ļ�ѧ����ʽ��![]() ��
��
��6��L�Ľṹ��ʽ�� ��
��

����Ŀ�����и������ʷ�����ȷ����
�� | �� | �� | ������ | |
A | ���� | ���� | ������ | �ɱ� |
B | ���� | �ռ� | ���� | ����ͭ |
C | ̼�� | ��ʯ�� | С�մ� | �������� |
D | ������̼ | ������ | ʳ�� | ʯ��ʯ |
A.AB.BC.CD.D



