题目内容
(1)(4分)下图表示在密闭容器中反应:2SO2+O2 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;

(2)(3分)已知下列两个热化学方程式:
H2(g)+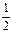 O2(g) = H2O( l ) △H=-285.8 kJ·mol-1
O2(g) = H2O( l ) △H=-285.8 kJ·mol-1
C3H8(g)+5O2(g) = 3CO2(g) +4H2O(l) △H=-2220.2 kJ·mol-1
实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热3847kJ,则混合气体中H2和C3H8的体积比是
(3)、(3分)实验室进行电解氯化钠溶液时,两极共收集到4.48L气体(标况),假设反应后溶液的总体积为200ml,则电解后溶液中氢氧化钠的物质的量浓度
 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;
(2)(3分)已知下列两个热化学方程式:
H2(g)+
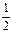 O2(g) = H2O( l ) △H=-285.8 kJ·mol-1
O2(g) = H2O( l ) △H=-285.8 kJ·mol-1C3H8(g)+5O2(g) = 3CO2(g) +4H2O(l) △H=-2220.2 kJ·mol-1
实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热3847kJ,则混合气体中H2和C3H8的体积比是
(3)、(3分)实验室进行电解氯化钠溶液时,两极共收集到4.48L气体(标况),假设反应后溶液的总体积为200ml,则电解后溶液中氢氧化钠的物质的量浓度
(1)升高温度 减少SO3的浓度(各2分)
(2)3:1 (3分) (3)1mol/l(3分)
(2)3:1 (3分) (3)1mol/l(3分)
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 qZ(g) ΔH>0,m+n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是
qZ(g) ΔH>0,m+n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是  2CO(正反应吸热),反应速率为v1:N2+3H2
2CO(正反应吸热),反应速率为v1:N2+3H2  2C(气) △H﹤0正确的说法是
2C(气) △H﹤0正确的说法是 2W。在反应过程中W的物质的量分数随温度变化如图所示:
2W。在反应过程中W的物质的量分数随温度变化如图所示: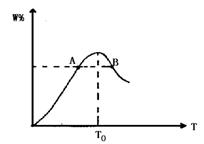
 △H=akJ/mol.
△H=akJ/mol. △H=bkJ/mol,
△H=bkJ/mol,