题目内容
向0.1 mol/L的氨水溶液中加水稀释或加入少量NH4Cl固体时均会引起变化的是
- A.溶液的导电能力减弱
- B.溶液的pH变小
- C.NH3·H2O的电离度变大
- D.Kw(水的离子积常数)变大
B
氨水的电离平衡:NH3·H2O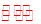
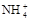 +OH—,稀释右移,电离度增大,各离子浓度减少,导电能力减弱,碱性减弱,PH增大;加NH4Cl固体,由于同离子效应,平衡左移,电离度减小,碱性减弱,PH增大,但加入电解质后可移动离子浓度增大,导电能力减弱。故答案为B
+OH—,稀释右移,电离度增大,各离子浓度减少,导电能力减弱,碱性减弱,PH增大;加NH4Cl固体,由于同离子效应,平衡左移,电离度减小,碱性减弱,PH增大,但加入电解质后可移动离子浓度增大,导电能力减弱。故答案为B
氨水的电离平衡:NH3·H2O
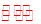
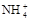 +OH—,稀释右移,电离度增大,各离子浓度减少,导电能力减弱,碱性减弱,PH增大;加NH4Cl固体,由于同离子效应,平衡左移,电离度减小,碱性减弱,PH增大,但加入电解质后可移动离子浓度增大,导电能力减弱。故答案为B
+OH—,稀释右移,电离度增大,各离子浓度减少,导电能力减弱,碱性减弱,PH增大;加NH4Cl固体,由于同离子效应,平衡左移,电离度减小,碱性减弱,PH增大,但加入电解质后可移动离子浓度增大,导电能力减弱。故答案为B 
练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目