题目内容
某溶液中含有HCO3-、SO32-、CO32-、CH3COO-等4种阴离子。向其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化) ( )
| A.CH3COO- | B.SO32- | C.CO32- | D.HCO3- |
A
考查离子共存问题
Na2O2溶于水后发生如下反应:2Na2O2+2H2O=4NaOH+O2↑
由于SO32-还原性较强,可被氧化,浓度减小;
HCO3-与OH-中和生成CO32-:HCO3-+OH-=CO32-+H2O,导致HCO3-浓度减小,而CO32浓度增大;
而溶液中离子浓度基本保持不变的是CH3COO-,故答案为A
Na2O2溶于水后发生如下反应:2Na2O2+2H2O=4NaOH+O2↑
由于SO32-还原性较强,可被氧化,浓度减小;
HCO3-与OH-中和生成CO32-:HCO3-+OH-=CO32-+H2O,导致HCO3-浓度减小,而CO32浓度增大;
而溶液中离子浓度基本保持不变的是CH3COO-,故答案为A

练习册系列答案
相关题目

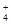 、Al3+、SO
、Al3+、SO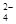 、NO
、NO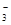
 、NO
、NO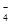 、SO
、SO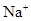 、
、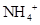 、
、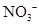 、
、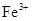
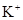 、CO32-、
、CO32-、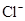 、
、
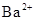 、
、 、
、