题目内容

(1)反应达到平衡时,放出的热量 。
A.小于92.2 kJ B.等于92.2 kJ C.大于92.2 kJ
(2)保持同一温度,在相同的容器中,若起始时加入2 mol NH3、1mol H2及固体催化剂,反应达到平衡时NH3的体积分数 。
A.等于0.25 B.大于0.25 C.小于0.25
(3)保持同一温度,在相同的容器中,起始通入一定物质的量N2、H2、NH3,欲使平衡时NH3的体积分数一定等于0.25。且起始时向正反应方向进行,
则充入N2的物质的量a(mol)的取值范围是 。
(4)右图是Tl℃时容器中NH3的物质的量随时间的变化曲线,
请在该图中补画出该反应在T2℃(T2>T1)时n(NH3)的变化
曲线。
(1)B(1分) (2)C(1分) (3)1mol<a<2mol(2分)
(4)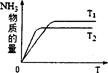 (2分)
(2分)
(4)
 (2分)
(2分)本题考查化学平衡的有关计算,(1)设反应消耗了amol的N2,则有
N2(g ) + 3H2(g) 2NH3(g);
2NH3(g);
起始量 2 mol 8 mol 0 mol
变化量 amol 3amol 2amol
平衡量 (2-a)mol (8-3a)mol 2amol
由题意可得:(10-2a)/10=80%,得a=1,即消耗了1mol的N2,生成了2molNH3,放出热量为92.2 kJ,B正确;
(2)将氨气按反应转化为反应物,则相当于起始量为1molN2和4molH2,相当于上述起始量的一半,则压强是原来的一半,压强减小,平衡向逆反应方向移动,NH3的百分含量减小,即小于2/8=25%,选C。
(3)达平衡时,N2、H2、NH3的量分别为1molN2、5molH2、2molNH3,要使反应向起反应方向进行,则起始的N2的量应大于1mol,由于是恒温恒容体积不相等反应的等效平衡,经转化后,所有对应量要相等,故N2的投入量不能超过2mol,即1mol<a<2mol。
(4)由于T2>T1,平衡向逆反应方向移动,平衡时NH3的百分含量减小,但温度升高,速率增大,达到平衡的时间缩短,故图象为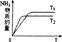 。
。
N2(g ) + 3H2(g)
 2NH3(g);
2NH3(g);起始量 2 mol 8 mol 0 mol
变化量 amol 3amol 2amol
平衡量 (2-a)mol (8-3a)mol 2amol
由题意可得:(10-2a)/10=80%,得a=1,即消耗了1mol的N2,生成了2molNH3,放出热量为92.2 kJ,B正确;
(2)将氨气按反应转化为反应物,则相当于起始量为1molN2和4molH2,相当于上述起始量的一半,则压强是原来的一半,压强减小,平衡向逆反应方向移动,NH3的百分含量减小,即小于2/8=25%,选C。
(3)达平衡时,N2、H2、NH3的量分别为1molN2、5molH2、2molNH3,要使反应向起反应方向进行,则起始的N2的量应大于1mol,由于是恒温恒容体积不相等反应的等效平衡,经转化后,所有对应量要相等,故N2的投入量不能超过2mol,即1mol<a<2mol。
(4)由于T2>T1,平衡向逆反应方向移动,平衡时NH3的百分含量减小,但温度升高,速率增大,达到平衡的时间缩短,故图象为
 。
。
练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
 Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是( )
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是( ) 2NH3。下列有关说法正确的是( )
2NH3。下列有关说法正确的是( )
 CO2(g)+H2(g),起始时只有CO、H2O(g)且浓度都是4 mol·L-1,达到平衡时,CO的浓度为1 mol·L-1;将H2O(g)的浓度提高到3 mol·L-1,平衡时CO的浓度为0.53 mol ·L-1。求:两次平衡时CO、H2O的转化率和CO2在平衡混合物中百分含量。
CO2(g)+H2(g),起始时只有CO、H2O(g)且浓度都是4 mol·L-1,达到平衡时,CO的浓度为1 mol·L-1;将H2O(g)的浓度提高到3 mol·L-1,平衡时CO的浓度为0.53 mol ·L-1。求:两次平衡时CO、H2O的转化率和CO2在平衡混合物中百分含量。 2C,达到化学平衡状态,经测得平衡时:c(A2)="0.5" mol·L-1,c(B2)="0.1" mol·L-1,c(C)="1.6" mol·L-1,若A2,B2,C的起始浓度分别用a mol·L-1,b mol·L-1,c mol·L-1表示,要维持相同的平衡状态,请计算后完成下列问题:
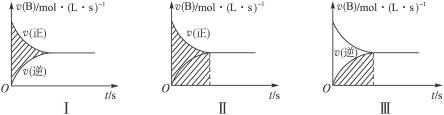
2C,达到化学平衡状态,经测得平衡时:c(A2)="0.5" mol·L-1,c(B2)="0.1" mol·L-1,c(C)="1.6" mol·L-1,若A2,B2,C的起始浓度分别用a mol·L-1,b mol·L-1,c mol·L-1表示,要维持相同的平衡状态,请计算后完成下列问题: 2C(g)以B的浓度改变表示的反应速率v(正)、v(逆)与时间的关系如下图所示。已知v的单位为mol·(L·s)-1,则图Ⅲ中阴影部分的面积可表示( )
2C(g)以B的浓度改变表示的反应速率v(正)、v(逆)与时间的关系如下图所示。已知v的单位为mol·(L·s)-1,则图Ⅲ中阴影部分的面积可表示( )