题目内容
17.下列离子方程式书写正确的是( )| A. | 氯化铁溶液中通入硫化氢气体:2Fe3++S2-═2Fe2++S↓ | |
| B. | 碳酸钡中加入稀硫酸BaCO3+2H+═Ba2++CO2↑+H2O | |
| C. | 碳酸钙跟醋酸反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ | |
| D. | 碳酸氢钠溶液中加入过量氢氧化钠溶液:HCO3-+OH-═CO32-+H2O |
分析 A.发生氧化还原反应生成氯化亚铁、S和水;
B.反应生成硫酸钡、水、二氧化碳;
C.反应生成醋酸钙、水、二氧化碳;
D.反应生成碳酸钠和水.
解答 解:A.氯化铁溶液中通入硫化氢气体的离子反应为2Fe3++H2S═2Fe2++S↓+2H+,故A错误;
B.碳酸钡中加入稀硫酸的离子反应为SO42-+BaCO3+2H+═BaSO4+CO2↑+H2O,故B错误;
C.碳酸钙跟醋酸反应的离子反应为CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑,故C正确;
D.碳酸氢钠溶液中加入过量氢氧化钠溶液的离子反应为HCO3-+OH-═CO32-+H2O,故D正确;
故选CD.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,注意电子、电荷守恒分析,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
7.氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子构型为平面三角形,则其阳离子的构型和阳离子中氮的杂化方式为( )
| A. | 直线 sp杂化 | B. | V型 sp杂化 | ||
| C. | 三角锥形 sp2杂化 | D. | 平面三角形 sp2杂化 |
5.想一想,NaOH固体,P2O5固体,无水CaCl2为什么可以归为一类?据此,与这三种物质可归为一类的是( )
| A. | 10%的H2SO4溶液 | B. | NaCl | ||
| C. | 碱石灰(固体,含NaOH,CaO) | D. | Ca(OH)2 |
12.标准状况下,由甲烷和乙烯组成的混合气体,其密度为1g•L-1,则该混合气体中甲烷与乙烯的质量比为( )
| A. | 1:2 | B. | 2:1 | C. | 7:8 | D. | 8:7 |
2.KMnO4稀溶液是一种常用的消毒剂,其消毒机理与( )相同.
| A. | NaClO溶液 | B. | 双氧水 | C. | 苯酚 | D. | 75%的酒精 |
5.已知可逆反应aA+bB?cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( )
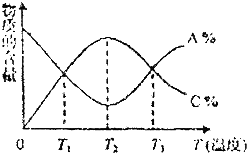

| A. | 该反应在T1、T3温度时达到过化学平衡 | |
| B. | 该反应的正反应是吸热反应 | |
| C. | 该反应在T2温度时达到过化学平衡 | |
| D. | 升高温度,平衡会向正反应方向移动 |
2.在一定温度下,硫酸铜晶体的培养皿中存在下列平衡:Cu2++SO42-+x H2O?CuSO4•xH2O,当向硫酸铜溶液中加少量无水硫酸铜粉末后,下列说法中正确的是( )
| A. | 溶液中Cu2+浓度增大 | B. | 溶液中Cu2+数目减少 | ||
| C. | 该硫酸铜晶体体积增大 | D. | 溶液的蓝色变浅 |
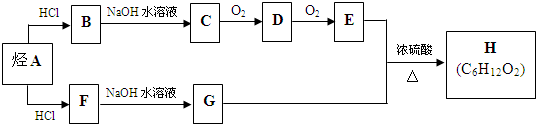
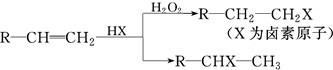
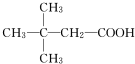 .(用结构简式表示)
.(用结构简式表示) .
.