题目内容
氮是大气中含量最多的气体,研究氮及其化合物对人类有重要的意义。
(1)合成氨的原理为:N2(g)+3H2 2NH3 △H=" -" 92.4kJ/mol
2NH3 △H=" -" 92.4kJ/mol
①将一定量的N2(g)和H2(g)放入1L的密闭容器中,在500℃、2×107Pa下达到平衡,平衡时测得N2为0.1 mol,H2为0.3 mol,NH3为0.1 mol。该条件下H2的转化率为 。
此温度下该反应的平衡常数K= 。
②欲提高H2的转化率,下列措施可行的是 。
a.向容器中按原比例再充入原料气
b.向容器中再充入惰性气体
c.改变反应的催化剂
d.液化生成物分离出氨
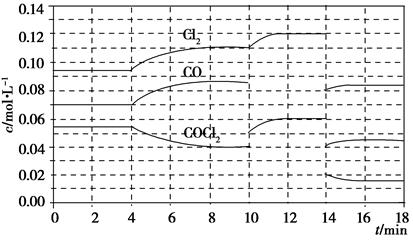
(2)在2L密闭容器中,800℃时反应2NO(g)+O2(g)  2NO2(g) △H<0体系中,各成分浓度随时间的变化如图:
2NO2(g) △H<0体系中,各成分浓度随时间的变化如图:
①用O2表示从0~2s内该反应的平均速率v=___________。
②能说明该反应已经达到平衡状态的是_________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变
③为使该反应的反应速率增大,且平衡向正反应方向移动的是_________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
(3)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。4CO(g)+2NO2(g) 4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是______(填代号)。
4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是______(填代号)。
(1)33.3% (2分) K=3.7(L/mol)2或100/27(L/mol)2(2分)②ad(2分)
(2)① 1.5×10-3mol/(L·s)(2分) ②b c (2分) ③c(1分)
(3)乙 (1分)
解析试题分析:⑴ ① N2(g) + 3H2  2NH3 △H=-92.4kJ/mol
2NH3 △H=-92.4kJ/mol
起始浓度:0.15mol/L 0.45mol/L 0
变化量: 0.05mol/L 0.15mol/L 0.1mol/L
平衡浓度:0.1mol/L 0.3mol/L 0.1mol/L
因此该条件下H2的转化率为:
平衡常数为:
②a.向容器中按原比例再充入原料气,可以引入假想状态,让按原比例充入的原料气充入一个体积相等,温度相等的容器中与原来的达到等效平衡,然后将这两个容器等压下合并,此刊转化率不变,这时,将容器压缩至原来的体积,相当于增大压强,平衡向右移动,氢气转化率增大; b.向容器中再充入惰性气体,容器体积不变,各组分的浓度不变,平衡不发生移动,氢气的转化率是不变的;c.改变反应的催化剂,只能改变化学反应的速率,不能改变各种物质的转化率;d.液化生成物分离出氨,减小了生成物的浓度,平衡正向移动,增大了氢气的转化率。
⑵①从图中三条线的变化趋势经及变化量的大小,可知a线对应的是二氧化氮;b线对应的是一氧化氮;c线对应的是氧气。所以: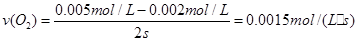
②a.v(NO2)=2v(O2) 这种关系是始终存在的,不能作为反应达到平衡的标志;b.容器内压强保持不变,表明容器内的各组分的总的分子数不变了,若正向移动,是分子总数减小的方向,若逆向移动,是分子总数增大的方向,因此,当容器内压强保持不变的时候,表明达到了平衡状态;c.v逆(NO)=2v正(O2):
①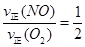 ,这个关系在反应中是始终存在的;若达到平衡状态,则有:②
,这个关系在反应中是始终存在的;若达到平衡状态,则有:② ,将②代入①可得:
,将②代入①可得: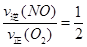 ,也就是v逆(NO)=2v正(O2),正确;d.容器内的密度保持不变,这是一个体积不变的气体之间的反应,不管反应到什么程度,容器内的密度始终保持不变,因此该选项不能作为反应达到平衡状态的标志。因此该题选bc。③a.及时分离出NO2气体,会使得反应速率减慢,错误;b.适当升高温度,反应速率加快,但反应逆向移动,错误;c.增大O2的浓度,反应速率加快,平衡逆向移动,正确;d.选择高效的催化剂,反应速率加快,但平衡不移动,错误。
,也就是v逆(NO)=2v正(O2),正确;d.容器内的密度保持不变,这是一个体积不变的气体之间的反应,不管反应到什么程度,容器内的密度始终保持不变,因此该选项不能作为反应达到平衡状态的标志。因此该题选bc。③a.及时分离出NO2气体,会使得反应速率减慢,错误;b.适当升高温度,反应速率加快,但反应逆向移动,错误;c.增大O2的浓度,反应速率加快,平衡逆向移动,正确;d.选择高效的催化剂,反应速率加快,但平衡不移动,错误。
⑶甲图中,在第一次达到平衡后,升高温度到T2,正逆反应速率都是增大的,因此甲错误;乙图中,遵循“先拐先平,数值大”,且在高温时,正向是放热的,升温平衡会逆向移动,使得二氧化氮的转化率减小。乙图正确;丙图中随着压强的增大,平衡正向移动,一氧化碳的转化率增大,但含量逐渐的降低。丙图错误。
考点:考查化学反应速率、化学平衡及其移动。

大气中的部分碘源于O3对海水中I-的氧化。将O3持续通入NaI溶液中进行模拟研究。
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g)=IO-(aq)+O2(g)ΔH1
②IO-(aq)+H+(g)=HOI(aq)ΔH2
③HOI(aq)+I-(aq)+H+(aq)=I2(aq)+H2O(l)ΔH3
总反应的化学方程式为_________________________________,
其反应热ΔH=______________。
(2)在溶液中存在化学平衡:I2(aq)+I-(aq)  I3-(aq),其平衡常数表达式为________。
I3-(aq),其平衡常数表达式为________。
(3)为探究Fe2+对O3氧化I-反应的影响(反应体系如图1),某研究小组测定两组实验中I3-浓度和体系pH,结果见图2和下表。
| 编号 | 反应物 | 反应前pH | 反应前pH |
| 第1组 | O3+I- | 5.2 | 11.0 |
| 第2组 | O3+I-+Fe2+ | 5.2 | 4.1 |
①第1组实验中,导致反应后pH升高的原因是______________。
②图1中的A为________。由Fe3+生成A的过程能显著提高I-的转化率,原因是____________________。
③第2组实验进行18 s后,I3-浓度下降。导致下降的直接原因有(双选)________。
A.c(H+)减小
B.c(I-)减小
C.I2(g)不断生成
D.c(Fe3+)增加
(4)据图2,计算3~18 s内第2组实验中生成I3-的平均反应速率(写出计算过程,结果保留两位有效数字)。
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义
(1)硫酸生产过程中2SO2(g)+O2(g) 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据下图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据下图回答下列问题: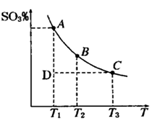
①2SO2(g)+O2(g) 2SO3(g)的△H__________0(填“>”或“<”),
2SO3(g)的△H__________0(填“>”或“<”),
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是 。
| A.体系的密度不发生变化 | B.SO2与SO3的体积比保持不变 |
| C.体系中硫元素的质量百分含量不再变化 | D.单位时间内转移4 mol 电子,同时消耗2 mol SO3 |
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g)
 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。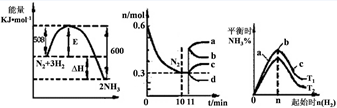
图1 图2 图3
①该反应的平衡常数表达式为 ,升高温度,平衡常数 (填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
(3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈 性,所得溶液中c(H+)- c(OH-)= (填写表达式)(已知:H2SO3:Ka1=1.7×10-2,Ka2=6.0×10-8,NH3·H2O:Kb=1.8×10-5)
在1.0 L密闭容器中放入0.10 mol A(g),在一定温度进行如下反应:
A(g)??B(g)+C(g) ΔH=+85.1 kJ·mol-1
ΔH=+85.1 kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/100 kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为____________________。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为______________。平衡时A的转化率为__________,列式并计算反应的平衡常数K__________________。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n(总)=________ mol,n(A)=________ mol。
②下表为反应物A浓度与反应时间的数据,计算:a=________。
| 反应时间t/h | 0 | 4 | 8 | 16 |
| c(A)/(mol·L-1) | 0.10 | a | 0.026 | 0.006 5 |
分析该反应中反应物的浓度c(A)变化与时间间隔(Δt)的规律,得出的结论是________________________________,由此规律推出反应在12 h时反应物的浓度c(A)为__________ mol·L-1。
把大气中的游离态的氮转化为氮的化合物的过程称为固氮。生物固氮和大气固氮(闪电时N2转化为NO)属于自然固氮,这远不能满足人类的需要。工业固氮(合成氨)是目前人工固氮的主要方法。有关大气固氮和工业固氮的平衡常数K值分别如下表一和表二。
表一:N2+ O2  2NO
2NO
| 温度 | 27℃ | 2000℃ |
| K值 | 3.84×10-31 | 0.1 |
表二:N2+ 3H2
 2NH3
2NH3 | 温度 | 25℃ | 350℃ | 400℃ | 450℃ |
| K值 | 5×108 | 1.847 | 0.507 | 0.152 |
A、N2+ O2
 2NO是吸热反应
2NO是吸热反应B、人类大规模模拟大气固氮是没有意义的
C、在常温下,增加工业固氮的容器的压强,K值会发生改变
D、工业固氮是放热反应
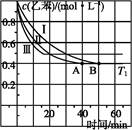
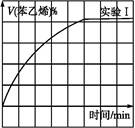
(2)向某密闭容器中加入4 mol NH3、1.2 mol H2和一定量的N2三种气体,一定条件下发生反应,各物质的浓度随时间变化如甲图所示[已知0~t1阶段保持恒温、恒容,且c(N2)未画出]。乙图为t2时刻后改变反应条件,反应速率随时间的变化情况,已知在t2、t3、t4、t5时刻各改变一种不同的条件。

①若t1="15" s,则t0~t1阶段的反应速率为v(H2)=
②N2的起始物质的量为
③反应达到平衡状态,下列说法中能表明已达到平衡状态的是
A、单位时间内生成a molN2,同时生成3a mol H2 B、容器的总压强不再变化
C、混合气体的密度不再变化 D、三个H—H 键断裂的同时有六个H—N键断裂
④t4时刻改变的条件为 ,t5时刻改变的条件为
⑤已知t0~t1阶段该反应放出或吸收的热量为Q kJ(Q为正值),试写出该反应的热化学方程式:____________________________________________________________________
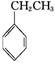 (g)+CO2(g)
(g)+CO2(g)
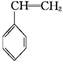 (g)+CO(g)+H2O(g) ΔH="-166" kJ·mol-1
(g)+CO(g)+H2O(g) ΔH="-166" kJ·mol-1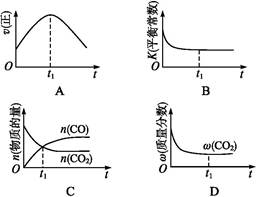
 2NH3 (g) △H=" -" 92.4kJ/mol
2NH3 (g) △H=" -" 92.4kJ/mol 2NO2(g)△H<0体系中,各成分浓度随时间的变化如图:
2NO2(g)△H<0体系中,各成分浓度随时间的变化如图:
 4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1