题目内容
19.下列实验操作正确的是( )| 编号 | 实验 | 操作 |
| A | 钠与水反应 | 用镊子从煤油中去除金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 配制一定浓度的碳酸钠溶液1000mL | 准确称取碳酸的固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀、定容 |
| C | 排除碱式滴定管尖嘴部分的气泡 | 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
| D | 去除分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出至截面上,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端放出 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.用镊子从煤油中去除金属钠,需要滤纸吸干煤油;
B.固体不能在容量瓶中溶解;
C.将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,利用液体的排出气泡;
D.分液时,避免上下层液体混合.
解答 解:A.用镊子从煤油中去除金属钠,需要滤纸吸干煤油,然后再切下绿豆大小的钠,小心放入装满水的烧杯中,否则煤油燃烧爆炸发生危险,故A错误;
B.固体不能在容量瓶中溶解,应在烧杯中溶解、冷却后转移到容量瓶中,故B错误;
C.将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,利用液体的排出气泡,操作合理,故C正确;
D.分液时,避免上下层液体混合,则下层液体从分液漏斗下端管口放出至截面上,关闭活塞,换一个容器,上层液体从分液漏斗上端倒出,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及实验基本操作、物质性质实验、溶液配制及分液等,把握物质的性质及实验技能为解答的关键,侧重分析与实验能力考查,注意实验评价性分析,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
9.下列排列顺序错误的是( )
| A. | 非金属性:S>Cl>F | B. | 碱性:NaOH>Mg( 0H)2>Al( 0H)3 | ||
| C. | 稳定性:PH3<H2S<HF | D. | 离子半径:02->Na+>Mg2+ |
4.如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )


| A. | X的某种单质是一种新型自来水消毒剂 | |
| B. | 简单离子半径:W->R2->X2->S3+ | |
| C. | R、Z不可能形成离子化合物 | |
| D. | 字母所代表的元素中最高价氧化物的水化物酸性最强的是Y |
11.已知下列热化学方程式:
Zn(s)+O2(g)═ZnO(s)△H=-Q1 kJ/mol
Hg(l)+O2(g)═HgO(s)△H=-Q2kJ/mol
Zn(s)+HgO(s)═Hg(l)+ZnO(s)△H=-Q3kJ/mol
Q3值为( )
Zn(s)+O2(g)═ZnO(s)△H=-Q1 kJ/mol
Hg(l)+O2(g)═HgO(s)△H=-Q2kJ/mol
Zn(s)+HgO(s)═Hg(l)+ZnO(s)△H=-Q3kJ/mol
Q3值为( )
| A. | Q2-Q1 | B. | Q1+Q2 | C. | Q1-Q2 | D. | -Q1-Q2 |
8.下列方法或操作正确且能达到预期目的是( )
| 序号 | 实验目的 | 方法及操作 |
| ① | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| ② | 鉴别二甲醚和乙醇 | 利用质谱法 |
| ③ | 检验乙醇在浓硫酸催化下的消去产物 | 将产物通入酸性KMnO4溶液 |
| ④ | 检验溴乙烷中的溴元素 | 将少量溴乙烷与NaOH溶液混合共热,充分反应并冷却后,再滴加AgNO3溶液 |
| ⑤ | 鉴别苯、四氯化碳、丙醛 | 分别滴加溴水 |
| A. | ①⑤ | B. | ②③ | C. | ①④⑤ | D. | ②③④ |
9.制备Fe3O4纳米颗粒的化学方程式为:3Fe2++2S2O32-+O2+4OH-=Fe3O4+X+2H2O.下列有关说法不正确的是( )
| A. | 上式中的X为S4O62- | |
| B. | 该反应中的还原剂为Fe2+和S2O32- | |
| C. | 当3 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1 mol | |
| D. | 当生成1 mol Fe3O4时,转移电子的物质的量为4 mol |

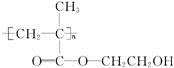 .
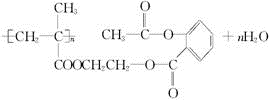
.
 .
.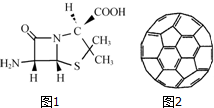 在人类文明的历程中,许多物质发挥过重要作用,如铁、硝酸钾、青霉素、聚乙烯、二氧化硅、富勒烯、含铬物质等.
在人类文明的历程中,许多物质发挥过重要作用,如铁、硝酸钾、青霉素、聚乙烯、二氧化硅、富勒烯、含铬物质等.
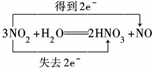 .
.