题目内容
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,而辛是由C元素形成的单质.已知:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1mol/L丁溶液的pH为13,则下列说法正确的是( )
| A、元素C形成的单质可以在点燃条件分别与元素A、B、D形成的单质化合,所得化合物均存在共价键 | B、元素B、C、D的原子半径由大到小的顺序为:r(D)>r(C)>r(B) | C、1.0 L 0.1 mol/L戊溶液中含阴离子总的物质的量小于0.1 mol | D、1 mol甲与足量的乙完全反应共转移约1.204×1024个电子 |
分析:0.1 mol/L 丁溶液的pH为13(25℃),丁是一元强碱,其含有的金属元素在短周期,则丁应为NaOH,发生反应:甲+乙=丁+辛,根据元素守恒可知,甲、乙两种物质至少共含有H、O、Na元素,辛是由C组成的单质,由发生反应可知,辛不能是Na,结合原子数可知,A为H、C为O、D为Na元素,故辛为氧气,可知甲是Na2O2、乙是水,再根据反应:甲+丙=戊+辛,可知丙是二氧化碳,戊是碳酸钠,则B为碳元素,结合对应单质、化合物的性质以及题目要求可解答该题.
解答:解:0.1 mol/L 丁溶液的pH为13(25℃),丁是一元强碱,其含有的金属元素在短周期,则丁应为NaOH,发生反应:甲+乙=丁+辛,根据元素守恒可知,甲、乙两种物质至少共含有H、O、Na元素,辛是由C组成的单质,由发生反应可知,辛不能是Na,结合原子数可知,A为H、C为O、D为Na元素,故辛为氧气,可知甲是Na2O2、乙是水,再根据反应:甲+丙=戊+辛,可知丙是二氧化碳,戊是碳酸钠,则B为碳元素,
A.氧气与氢气、碳反应生成化合物只含有共价键,氧气与Na在加热条件下反应生成过氧化钠,含有离子键、共价键,故A正确;
B.同周期随原子序数增大原子半径减小,同主族自上而下原子半径增大,故原子半径大小顺序为:Na>C>O,即:D>B>C,故B错误;
C.戊是碳酸钠,在碳酸钠溶液中,CO32-离子水解生成HCO3-离子和OH-离子,溶液中阴离子总的物质的量大于0.1mol,故C错误;
D.甲与足量的乙完全反应的方程式为:2Na2O2+2H2O═4NaOH+O2↑,反应中过氧化钠其氧化剂、还原剂作用,各占一半,故1molNa2O2反应转移的电子为1mol×
×2=1mol,约6.02×1O23个电子,故D错误,
故选A.
A.氧气与氢气、碳反应生成化合物只含有共价键,氧气与Na在加热条件下反应生成过氧化钠,含有离子键、共价键,故A正确;
B.同周期随原子序数增大原子半径减小,同主族自上而下原子半径增大,故原子半径大小顺序为:Na>C>O,即:D>B>C,故B错误;
C.戊是碳酸钠,在碳酸钠溶液中,CO32-离子水解生成HCO3-离子和OH-离子,溶液中阴离子总的物质的量大于0.1mol,故C错误;
D.甲与足量的乙完全反应的方程式为:2Na2O2+2H2O═4NaOH+O2↑,反应中过氧化钠其氧化剂、还原剂作用,各占一半,故1molNa2O2反应转移的电子为1mol×
| 1 |
| 2 |
故选A.
点评:本题考查元素化合物推断,题目难度中等,需要学生熟练掌握元素化合物知识,对学生的逻辑推理有一定的要求,C选项注意盐类水解.

练习册系列答案
相关题目
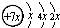 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:

 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为 ,下列比较中正确的是( )
,下列比较中正确的是( )