题目内容
13.NA为阿伏加德罗常数,C2H2(g)完全燃烧生成CO2和液态水的反应,有5NA个电子转移时,放出650kJ的热量,该反应的热化学方程式为2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600kJ•mol-1.分析 在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,0.5mol乙炔发生反应放出650kJ的热量,所以2mol乙炔完全反应有20NA个电子转移时,放出2600kJ的热量,依据热化学方程式书写方法写出,标注物质聚集状态和对应反应的焓变.
解答 解:在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,0.5mol乙炔发生反应放出650kJ的热量,所以2mol乙炔完全反应有20NA个电子转移时,放出2600kJ的热量,则热化学方程式为:2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600 kJ•mol-1,
故答案为:2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600 kJ•mol-1.
点评 本题考查热化学方程式的书写、盖斯定律、依据氧化还原反应电子转移计算反应热等,题目较简单,注意盖斯定律的理解与运用.

练习册系列答案
相关题目
3.二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚(CH3OCH3).
请回答下列问题:
(1)利用水煤气合成二甲醚的三步反应如下:(甲醇:CH3OH)
①2H2(g)+CO(g)═CH3OH(g);△H=-90.8kJ•mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g);△H=-23.5kJ•mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g);△H=-41.3kJ•mol-1
则利用水煤气合成二甲醚的总反应的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol-1.
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是ce(填字母代号).
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(2)、已知反应②2CH3OH(g)═CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v正> v逆 (填“>”、“<”或“=”).
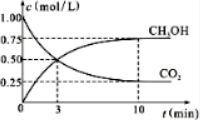
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=0.04mol/L;该时间内反应速率v(CH3OH)=0.16 mol/(L•min).
请回答下列问题:
(1)利用水煤气合成二甲醚的三步反应如下:(甲醇:CH3OH)
①2H2(g)+CO(g)═CH3OH(g);△H=-90.8kJ•mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g);△H=-23.5kJ•mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g);△H=-41.3kJ•mol-1
则利用水煤气合成二甲醚的总反应的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol-1.
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是ce(填字母代号).
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(2)、已知反应②2CH3OH(g)═CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=0.04mol/L;该时间内反应速率v(CH3OH)=0.16 mol/(L•min).
1.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H=-241.8 kJ•mol-1,则氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金刚石,s);△H=+1.9 kJ•mol-1,则石墨比金刚石稳定 | |
| C. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.3 kJ•mol-1,则含1mol NaOH的稀溶液与1mol的稀醋酸完全中和,放出的热量也等于57.3kJ | |
| D. | 已知2C(s)+2O2(g)═2CO2(g))△H=a kJ•mol-1、2C(s)+O2(g)═2CO(g)△H=b kJ•mol-1,则a>b |
18.我国卫星发射所用的长征2号火箭的主要燃料是偏二甲肼(C2H8N2),氧化剂是NO2,燃烧产物只有N2、CO2和H2O.有的国家用肼(N2H4)作为火箭发动机的燃料.NO2为氧化剂,反应生成N2和水蒸气.已知:N2(g)+2O2(g)═2NO2(g)△H=+67.7kJ•mol-1;N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534kJ•mol-1.下列关于肼和NO2反应的热化学方程式中正确的是( )
| A. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O (l)△H=+1135.7kJ•mol-1 | |
| B. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=-1135.7kJ•mol-1 | |
| C. | N2H4(g)+NO2(g)═$\frac{3}{2}$N2(g)+2H2O(g)△H=+1135.7kJ•mol-1 | |
| D. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g)△H=-1135.7kJ•mol-1 |
5.在密闭容器中,将1.0molCO与1.0molH2O混合加热到800℃,发生下列反应:CO(g)+H2O(g)?CO2(g)+H2(g).一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.则下列说法正确的是( )
| A. | 427℃时该反应的平衡常数为9.4,则该反应的△H>0 | |
| B. | 800℃下,该反应的化学平衡常数为0.25 | |
| C. | 同温下,若继续向该平衡体系中通入1.0mol的H2O(g),则平衡时H2O(g)转化率为66.7% | |
| D. | 同温下,若继续向该平衡体系中通入1.0mol的CO(g),则平衡时H2O(g)物质的量分数为11.1% |
3.下列化学方程式属氧化还原反应的是( )
| A. | H2S+CuSO4═H2SO4+CuS↓ | B. | H2SO4+CuO═CuSO4+H2O | ||
| C. | 2NaOH+CO2═Na2CO3+H2O | D. | Fe2O3+3CO═2Fe+3CO2↑ |