题目内容
【题目】化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图所示的反应。试写出:
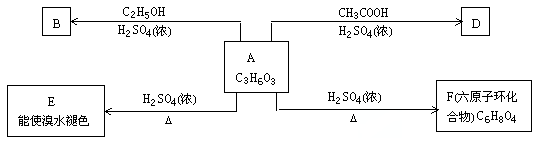
(1)化合物的结构简式:A ;B ;D
(2)化学方程式: A→E ;A→F
反应类型: A→E ;A→F
【答案】(1)![]()
![]()
![]()
(2)![]() +H2O
+H2O

反应类型:A→E消去(或脱水)A→F酯化(或分子向脱水)
【解析】
试题分析:(1)分析框图中的关系,A与乙醇在浓硫酸条件下生成B为酯化反应,说明A中有-COOH,A与乙酸在浓硫酸条件下生成D为酯化反应,说明A中有-OH,再结合A的分子式(C3H6O3)分析,A中的烃基为-C2H4-,则A的可能结构为:HOCH2CH2COOH,A在某种催化剂存在下进行氧化,其产物不能发生银镜反应,说明A中无-CH2OH的结构,所以A的结构简式为![]() ;则B的结构简式为
;则B的结构简式为![]() ,D的结构简式为
,D的结构简式为![]() 。
。
(2)E能使溴水褪色,说明含有不饱和的键,则A在浓硫酸条件下发生了醇的消去反应,所以A到E的化学方程式为![]() +H2O。
+H2O。
F为含有6个碳原子的环状化合物,A中只有3个碳原子,说明A到F为两分子A间的酯化反应,反应的化学方程式为 ;
;
根据上述分析,A→E的反应属于消去反应,A→F的反应属于酯化反应,

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案【题目】某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 , 仍存在的缺陷是 . 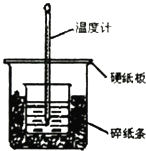
(2)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1 , 则△H1与△H的关系为:△H1△H(填“<”、“>”或“=”).
(3)写出该反应的中和热的热化学方程式(中和热为57.3kJ/mol): .
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,装置已做改进.实验数据如表.
起始温度/℃ | 终止温度/℃ | 温度差/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
2 | 24.5 | 24.2 | 24.35 | 27.6 | 3.25 |
3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
又已知0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都近似为1g/cm3 , 中和后生成溶液的比热容c=4.18J/(g℃).则中和热△H=(取小数点后一位).
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母) .
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把H2SO4溶液倒入盛有NaOH溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后未清洗直接测定H2SO4溶液的温度
e.实验当天气温较高.