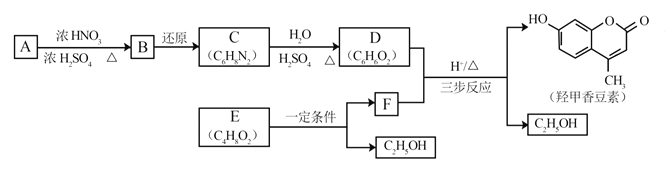
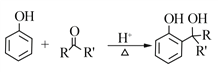
题目内容
【题目】【选修3:物质结构与性质】自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用。回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子核外电子排布式为_________,C、N、O三种元素的第一电离能由大到小的顺序为_________。
(2)在硫酸铜溶液中加入过量KCN能生成配离子[Cu(CN)4]2, 1 mol CN中含有的π键的数目为_________。与CN互为等电子体的分子有_______ (写出一种即可)。
(3)在络离子[Cu(NH3)4] 2+中 NH3 的 VSEPR 模型为____________,其中N原子的杂化轨道类型为_________。
(4)NaCl和MgO都属离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是_______________________。
(5)晶体是由无数晶胞___________而成。铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。则铁镁合金的化学式为______,若该晶胞的晶胞参数为d nm,则该合金的密度为______g/cm3 (不必化简,用NA表示阿伏加德罗常数)。

【答案】 [Ar]3d9 或 1s22s22p63s23p63d9 N > O >C 2NA或2×6.02×1023 CO或者 N2 四面体形 sp3 氧化镁晶体所含离子半径小,电荷多,晶格能大 无隙并置 Mg2Fe ![]()
【解析】(1)Cu2+核外有27个电子,根据核外电子排布规律,基态Cu2+的电子排布式是[Ar]3d9 。非金属性越强第一电离能越大,由于氮元素的2p轨道电子处于半充满状态,稳定性强,因此C、N、O三种元素的第一电离能由大到小的顺序为N>O>C。(2)CN中N原子含有孤对电子,CN中提供孤电子对的原子是N,CN-存在C、N叁键,叁键中有2个π键,1 mol CN含有的π键是2mol,数目为2×6.02×1023。等电子体是原子数相同、价电子数分别相同的分子或离子,与CN互为等电子体的分子有CO或者N2。(3)NH3的价层电子对数是![]() ,所以VSEPR 模型为四面体形,其中N原子的杂化轨道类型为sp3。(4)离子化合物的熔点与离子半径和电荷多少有关,氧化镁晶体所含离子半径小,电荷多,所以晶格能大。(5)晶体是由无数晶胞无隙并置而成。根据均摊原则晶胞中铁原子数
,所以VSEPR 模型为四面体形,其中N原子的杂化轨道类型为sp3。(4)离子化合物的熔点与离子半径和电荷多少有关,氧化镁晶体所含离子半径小,电荷多,所以晶格能大。(5)晶体是由无数晶胞无隙并置而成。根据均摊原则晶胞中铁原子数![]() =4,镁原子数8,,铁镁合金的化学式是Mg2Fe,设有1mol晶胞,体积为
=4,镁原子数8,,铁镁合金的化学式是Mg2Fe,设有1mol晶胞,体积为![]() ,质量为104
,质量为104![]() ,根据
,根据![]() 可知合金的密度是
可知合金的密度是![]() 。
。

【题目】某兴趣小组在实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,并探究溴乙烷的性质。反应原理和实验装置如下(加热装置未画出):
H2SO4(浓)+NaBr![]() NaHSO4+HBr↑ CH3CH2OH+HBr
NaHSO4+HBr↑ CH3CH2OH+HBr![]() CH3CH2Br+H2O
CH3CH2Br+H2O

有关数据见下表:
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红色液体 |
密度/(g·cm3) | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
Ⅰ.溴乙烷的制备:
(1)若图甲中A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应,其化学方程式为__________;F连接导管通入稀NaOH溶液中,其目的主要是_________;导管E的末端须低于D的水面,其目的是__________。
(2)为了除去粗产品中的氧化性杂质,宜选择下列_________ (填序号)溶液来洗涤所得粗产品。
A.氢氧化钠 B.碘化钾 C.碳酸氢钠 D.亚硫酸钠
(3)粗产品用上述溶液洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的无水硫酸镁固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0g。从乙醇的角度考虑,本实验所得溴乙烷的产率是___________。
Ⅱ.溴乙烷性质的探究
用如图乙实验装置(铁架台、酒精灯略)验证溴乙烷的性质:在试管中加入10mL6mol·L1NaOH溶液和2mL溴乙烷,振荡、静置,液体分层,水浴加热。
(4)观察到___________,表明溴乙烷与NaOH溶液已完全反应。
(5)为证明溴乙烷在NaOH乙醇溶液中反应的气体产物为乙烯,将生成的气体通入如图丙装置。a试管中的水的作用是 ___________,若无a试管,b试管中的试剂应为___________ 。