题目内容
下列是与硫元素相关的一系列实验:根据下图所示实验回答下列问题:
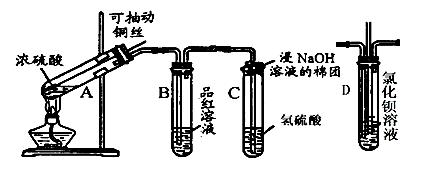
(1) 试管C口部的棉团上发生反应的离子方程式是 。
(2) 反应一段时间后,将B试管中的溶液加热,可以观察到 。试管C中溶液变浑浊,则证明SO2具有 性。
(3) 试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是 ,如果浸NaHCO3溶液,则发生反应的离子方程式是 。
(4) 如将B试管换成D试管,并从直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是 、 、 、 (要求填二种化合物和二种单质的化学式)。
(5) 取下C试管,试管中溶液浑浊,煮沸后,再加入Na2S溶液并加热,溶液变澄清,经测定溶液中主要存在一种摩尔质量为128g/mol的二价阴离子(反应①)。向该澄清液中加入氯水,溶液仍然澄清(反应②),加入氯化钡可得一种不溶于稀盐酸的白色沉淀,写出反应①和反应②的离子方程式 , 。

(1) 试管C口部的棉团上发生反应的离子方程式是 。
(2) 反应一段时间后,将B试管中的溶液加热,可以观察到 。试管C中溶液变浑浊,则证明SO2具有 性。
(3) 试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是 ,如果浸NaHCO3溶液,则发生反应的离子方程式是 。
(4) 如将B试管换成D试管,并从直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是 、 、 、 (要求填二种化合物和二种单质的化学式)。
(5) 取下C试管,试管中溶液浑浊,煮沸后,再加入Na2S溶液并加热,溶液变澄清,经测定溶液中主要存在一种摩尔质量为128g/mol的二价阴离子(反应①)。向该澄清液中加入氯水,溶液仍然澄清(反应②),加入氯化钡可得一种不溶于稀盐酸的白色沉淀,写出反应①和反应②的离子方程式 , 。
(1)SO2 +2OH-=SO32-+H2O (或SO2 +OH-=H SO3-) (2分)
(2) 溶液由无色变成红色 (1分) 氧化 (1分)
(3)吸收有害气体,防止污染空气 (1分)
HCO3-+SO2=HSO3-+CO2(或2HCO3-+SO2=SO32-+2CO2 +H2O) (2分)
(4)NH3 NO2 ClO2 Cl2 、O3 O2、Br2(g) I2(g)(3分)
(5)3S+S2- = S42-(3分) S42-+13Cl2+12H2O = 26Cl-+4SO42-+24H+(3分)
(2) 溶液由无色变成红色 (1分) 氧化 (1分)
(3)吸收有害气体,防止污染空气 (1分)
HCO3-+SO2=HSO3-+CO2(或2HCO3-+SO2=SO32-+2CO2 +H2O) (2分)
(4)NH3 NO2 ClO2 Cl2 、O3 O2、Br2(g) I2(g)(3分)
(5)3S+S2- = S42-(3分) S42-+13Cl2+12H2O = 26Cl-+4SO42-+24H+(3分)
略

练习册系列答案
相关题目

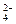 、CO
、CO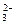 、Cl-。为了检验其中是否含有SO
、Cl-。为了检验其中是否含有SO ,写出每一实验鉴定离子的结论与理由。
,写出每一实验鉴定离子的结论与理由。