题目内容
【题目】某研究小组欲探究SO2的化学性质,设计了如下实验方案。
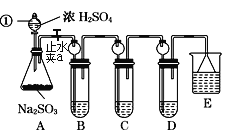
(1)指出仪器①的名称:___。
(2)装置B检验SO2的氧化性,则B中所盛试剂可以为___。
(3)装置C中盛装溴水用以检验SO2的___性,则C中反应的离子方程式为___。
(4)装置D中盛装新制漂白粉浓溶液,通入SO2一段时间后,D中出现了大量白色沉淀。同学们对白色沉淀成分提出三种假设:
①假设一:该白色沉淀为CaSO3;
假设二:该白色沉淀为___;
假设三:该白色沉淀为上述两种物质的混合物。
②基于假设一,同学们对白色沉淀成分进行了探究。设计如下方案:
限选的试剂:0.5mol·L-1HCl、0.5 mol·L-1H2SO4、0.5mol·L-1BaCl2、1mol·L-1NaOH、品红溶液。
第1步,将D中沉淀过滤、洗涤干净,备用。
请回答洗涤沉淀的方法:___。
第2步,用另一只干净试管取少量沉淀样品,加入___(试剂),塞上带导管的单孔塞,将导管的另一端插入盛有___的试管中。若出现固体完全溶解,出现气泡,且该溶液褪色现象,则假设一成立。
(5)装置E中盛放的试剂是__,作用是___。
【答案】分液漏斗 硫化氢溶液(或硫化钠、硫氢化钠溶液均可) 还原性 SO2+Br2+2H2O=SO42-+4H++2Br- CaSO4 沿玻璃棒向漏斗中加蒸馏水至浸没沉淀,待水流尽重复2到3次以上操作 过量0.5mol·L-1HCl 品红溶液 NaOH溶液 吸收多余的SO2,防止污染环境,造成大气污染
【解析】
探究SO2的化学性质,根据装置图,A装置是制取二氧化硫,装置B检验SO2的氧化性,装置C检验SO2的还原性,装置D探究二氧化硫和漂白粉的反应,装置E为尾气吸收装置。
(4)①新制漂白粉浓溶液中含有的次氯酸根离子具有氧化性,可能氧化亚硫酸根离子;②因沉淀的表面有可溶性的杂质,需用蒸馏水重复洗涤;亚硫酸钙和稀酸能够反应生成二氧化硫,可以借助于二氧化硫具有漂白性检验生成的二氧化硫,据此分析解答。
(1)根据图示,仪器①是分液漏斗,故答案为:分液漏斗;
(2)装置B需要检验SO2的氧化性,硫化氢水溶液或硫化钠、硫氢化钠溶液中的硫元素都为-2价,都能被二氧化硫氧化,体现二氧化硫的氧化性,故答案为:硫化氢水溶液(或硫化钠、硫氢化钠溶液);
(3)在反应Br2+SO2+2H2O═2HBr+H2SO4中,Br元素的化合价由0降低为-1价,则Br2为氧化剂,在反应中表现氧化性,S元素的化合价+4价升高+6价,则SO2为还原剂,在反应中表现还原性,离子方程式为:SO2+Br2+2H2O=SO42-+4H++2Br-,故答案为:还原;SO2+Br2+2H2O=SO42-+4H++2Br-;
(4)①新制漂白粉浓溶液中含有的次氯酸根离子具有强氧化性,二氧化硫具有还原性,会发生氧化还原反应,生成产物可能为硫酸钙,故答案为:CaSO4;
②白色沉淀表面有钙离子和氯离子、硫酸根离子等可溶性的离子,需除去这些离子,方法是沿玻璃棒向漏斗中加蒸馏水至浸没沉淀,待水流尽后重复2~3次以上操作;亚硫酸钙和盐酸反应CaSO3+2HCl═CaCl2+SO2↑+H2O,二氧化硫与品红化合生成无色物质,能使品红溶液褪色;因为出现固体完全溶解,因此不能选用0.5 mol·L-1H2SO4,故答案为:沿玻璃棒向漏斗中加蒸馏水至浸没沉淀,待水流尽后重复2到3次以上操作;过量(或适量)0.5 molL-1HCl;品红溶液;
(5)二氧化硫是有毒气体,属于大气污染物,所以装置E的作用是吸收二氧化硫,防止造成空气污染,可用氢氧化钠,氢氧化钠和二氧化硫反应2NaOH+SO2═Na2SO3+H2O,为防止倒吸,需用倒扣的漏斗,故答案为:NaOH溶液;吸收SO2,防止造成空气污染。

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案