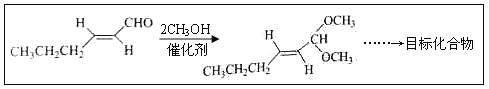
题目内容
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质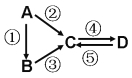 。它们之间有如下的反应关系:
。它们之间有如下的反应关系:
(1)若B是淡黄色固体,②③反应均用到同一种液态氢化物。D物质常用于食品工业。写出④反应的化学方程式
(2)若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。写出③反应的化学方程式
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出④反应离子方程式
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式
(5)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。写出④反应的离子方程式
【答案】(1)NaOH+CO2=NaHCO3
(2)4NH3+5O2=4NO+6H2O
(3)AlO-+CO2+2H2O=Al(OH)3↓+HCO3-
(4)Si+2NaOH+2H2O=NaSiO3+2H2↑
(5)2Fe3++Fe=3Fe2+
【解析】
试题分析:(1)若B是淡黄色固体,②③反应均用到同一种液态氢化物。D物质常用于食品工业。A是Na、B是Na2O2、C是NaOH、D是NaHCO3;④反应的化学方程式NaOH+CO2=NaHCO3
(2)若B是气态氢化物.C、D是氧化物且会造成光化学烟雾污染,判断为NO、NO2,推断A为N2,B为NH3,该反应的化学方程式4NH3+5O2=4NO+6H2O;
(3)若D物质具有两性推断D为Al(OH)3,④反应是通入过量的一种引起温室效应的主要气体,说明C为偏铝酸钠NaAlO2,②③反应均要用强碱溶液,判断A为Al,B为AlCl3,单质A为Al,元素在周期表中的位置是第三周期ⅢA族,④反应离子方程式:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-;
(4)若A是太阳能电池用的光伏材料,判断A为Si.C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性,说明盐水解呈碱性,C为Na2SiO3,D为Na2CO3,B为SiO2;反应②的化学方程式为:Si+2NaOH+2H2O=Na2SiO3+2H2↑;
(5)若A是应用最广泛的金属.推断为Fe,④反应用到A,②⑤反应均用到同一种非金属单质.推断为Cl2,判断C为FeCl3,D为FeCl2, 2Fe3++Fe=3Fe2+。

 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】中和热的测定是高中重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
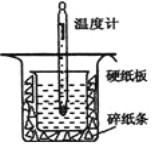
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________,除此之外,装置中的一个明显错误是 。
(2)若改用60mL 0.25mol·L-1 H2SO4和50mL 0.55mol·L-1NaOH溶液进行反应与上述实验相比,所放出的热量________ ___(填“相等”、“不相等”),若实验操作均正确,则所求中和热________ ___(填“相等”“不相等”)。
(3)实验数据如下表:
①请填写下表中的空白:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
|
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=______ ____ ( 取小数点后一位)。