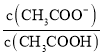题目内容
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
(实验目的)制取乙酸乙酯。
(实验原理)甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,浓硫酸的作用是_________、_________。
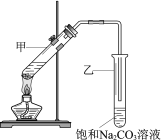
(装置设计)甲、乙、丙三位同学分别设计了下列三套实验装置:
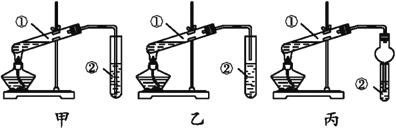
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是____(填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是_________。
(实验步骤)
(1)按选择的装置组装仪器,在试管中先加入3 mL乙醇和2 mL冰醋酸,并在摇动下缓缓加入2 mL的浓硫酸;
(2)将试管固定在铁架台上;
(3)在试管②中加入适量的饱和Na2CO3溶液;
(4)用酒精灯对试管①加热;
(5)当观察到试管②中有明显现象时停止实验。
(问题讨论)
a.按步骤(1)装好实验装置,加入样品前还应检查__________;
b.根据试管②中观察到的现象,可知乙酸乙酯的物理性质有_________;
c.试管②中饱和Na2CO3溶液的作用是________、________、________;
d.从试管②中分离出乙酸乙酯的实验操作是____。
【答案】催化剂 吸水剂 乙 防倒吸 装置的气密性 无色、不溶于水、密度比水小等 溶解乙醇 中和乙酸 降低乙酸乙酯的溶解度 分液
【解析】
[实验原理]乙酸和乙醇在浓硫酸作用下发生酯化反应,生成乙酸乙酯和水,浓硫酸有吸水性,促进该反应向正反应方向移动,浓硫酸能加快反应速率,所以浓硫酸作催化剂和吸水剂,
故答案为:催化剂;吸水剂;
[装置设计]乙酸和乙醇易溶于水,导管插入液面下容易发生倒吸,所以为了防止倒吸,导管不能插入液面以下,应该选乙装置;球形干燥管导气的同时也起到防倒吸作用,
故答案为:乙;防倒吸;
[问题讨论]a、实验前,要检查装置的气密性,否则会导致实验失败,故答案为:装置气密性;
b、乙酸乙酯在混合液上层,说明乙酸乙酯不溶于水、密度比水小,还能够闻到香味,说明乙酸乙酯具有特殊香味,
故答案为:无色;不溶于水(或密度比水小、具有特殊香味等);
c、碳酸钠溶液中的水溶解乙醇,碳酸钠能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液,
故答案为:中和乙酸;降低乙酸乙酯的溶解度;
d、乙酸乙酯不溶于饱和碳酸钠溶液,混合液会分层,分离乙酸乙酯的方法为分液,
故答案为:分液。

【题目】滴定是一种重要的定量实验方法:
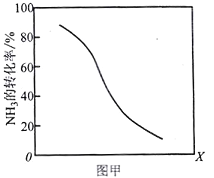
I. 常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:
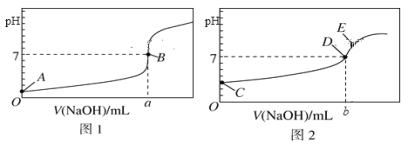
(1)滴定盐酸的曲线是图__________(填“1”或“2”)。
(2)滴定前CH3COOH的电离度为__________(电离度=![]() ×100%)。
×100%)。
(3)达到B、D状态时,反应消耗的NaOH溶液的体积a__________b(填“>”“<”或“=”);若图中E点pH=8,则c(Na+)-c(CH3COO-)的精确值为__________mol/L。
Ⅱ. 现使用酸碱中和滴定法测定市售白醋中醋酸的浓度
(1)实验步骤:
①量取10.00 mL市售白醋,在烧杯中用水稀释后转移到100 mL容量瓶中定容,摇匀得待测白醋溶液。
②用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴酚酞作指示剂。
③读取盛装0.1000 mol/L NaOH 溶液的碱式滴定管的初始读数。
④滴定。当___________________时,停止滴定,并记录NaOH溶液的最终读数。
⑤重复②、③、④步骤3次。
数据记录如下:
滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(2)数据处理:
根据实验数据计算,可得市售白醋中醋酸的浓度为_________ mol/L
(3)误差在本实验的滴定过程中,下列操作会使实验结果偏大的是_________。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后消失
c.锥形瓶中加入待测白醋溶液后,再加入少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
e.滴定前平视读数,滴定后俯视读数