题目内容
【题目】Ⅰ.有机物X是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究X的组成与结构,进行了如下实验:
(1)有机物X的质谱图为: | |
| 有机物X的相对分子质量是________。 |
(2)将10.0 g X在足量O2中充分燃烧,并使其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2 g,KOH浓溶液增重22.0 g。 | 有机物X的分子式是______。 |
(3)经红外光谱测定,有机物X中含有醛基;有机物X的核磁共振氢谱图上有2个吸收峰,峰面积之比是3∶1。 | 有机物X的结构简式是__________。 |
II.写出与![]() 互为同分异构体,且一溴代物只有两种的芳香烃的结构简式和名称:________________、___________。
互为同分异构体,且一溴代物只有两种的芳香烃的结构简式和名称:________________、___________。
【答案】 100 C5H8O2 (CH3)2C(CHO)2 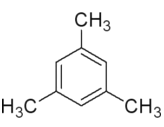 均三甲苯或1,3,5三甲苯
均三甲苯或1,3,5三甲苯
【解析】Ⅰ、(1)质谱图的最右端的曲线对应的横坐标就是有机物的相对分子质量,所以有机物X的相对分子质量是100。
(2) 10.0 g X的物质的量为0.1mol,生成的水的物质的量为7.2/18=0.4(mol),生成的CO2的物质的量为22/44=0.5(mol),所以X分子中含有5个碳原子和8个氢原子,设为C5H8Oz,则12×5+8+16×z=100,所以z=2,故分子式为C5H8O2。
(3) C5H8O2的不饱和度为2,一个醛基的不饱和度为1,X的核磁共振氢谱图上有2个吸收峰,峰面积之比是3∶1=6:2,可以判断出X结构中含有2个甲基和2个醛基,故其结构简式为(CH3)2C(CHO)2。
II、![]() 的分子式为C9H12,不饱和度为4,含有一个苯环,其余碳碳之间为单键,一定含有甲基。一溴代物只有两种,甲基上有一种一溴代物,则苯环上也只有1种一溴代物,故苯环上一定连着3个甲基,且处于苯环上1,3,5的位置,所以结构简式为
的分子式为C9H12,不饱和度为4,含有一个苯环,其余碳碳之间为单键,一定含有甲基。一溴代物只有两种,甲基上有一种一溴代物,则苯环上也只有1种一溴代物,故苯环上一定连着3个甲基,且处于苯环上1,3,5的位置,所以结构简式为 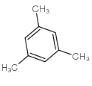 ,名称为:均三甲苯或1,3,5-三甲苯。
,名称为:均三甲苯或1,3,5-三甲苯。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】某学习小组为了探究Fe(NO3)3的热稳定性和氧化性,设计如下实验:
实验(一): 热稳定性
利用如图装置进行实验,加热A中Fe(NO3)3固体,A 和B中都有红棕色气体产生,A 试管中生成了红色粉末。
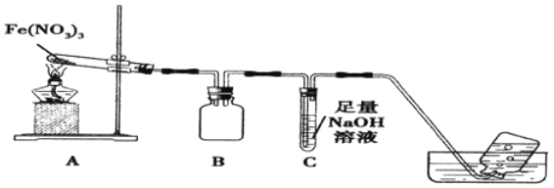
(1)B装置的作用____________;要检验A中红色固体是否为Fe2O3,应该选用的试剂是____________(填化学式)。
(2)加热A中试管一段时间后,C 中导管口有气泡产生,而集气瓶中无气泡产生原因是______________。
(3)写出硝酸铁受热分解的化学方程式__________________。
实验(二):氧化性
Fe3+和Ag+的氧化性相对强弱一直是实验探究的热点。该小组设计如下实验:
试验编号 | 实验操作 | 现象 |
a | 向10mL3mol·L-1KNO3酸性溶液(pH=1)中插入一根洁净的银丝,并滴加氯化钠溶液 | 无沉淀生成 |
b | 向10mL3mol·L-1AgNO3溶液中滴加2mL0.1mol·L-1FeSO4溶液,振荡;再滴加酸性高锰酸钾溶液 | 紫红色溶液不褪色 |
c | 向10 mL3mol·L-1Fe(NO3)3溶液(pH=1)中插入一根洁净的银丝,并滴加氯化钠溶液 | 产生白色沉淀 |
(4)设计实验a的目的是_____________________;实验c的结论是_____________________________。
(5)实验b涉及反应的离子方程式为____________________________________。
(6)实验结论是Fe3+、Ag+氧化性的相对强弱与离子的_____________________有关。