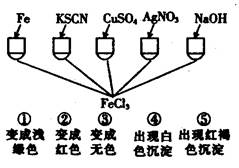
��Ŀ����
�ӻ�ͭ��Cu2S�������û���ͭ������ȡͭ���������·�Ӧ��

��������Cu2Sұ��ͭ����ȡCuSO4��5H2O������ͼ��

��Cu2S��ͭԪ�صĻ��ϼ�Ϊ ������1molCu2S��O2��Ӧ����2molCuʱ��ת�Ƶ��ӵ����ʵ����� ��
��Cu2O��CuO�м�������ϡ����õ�����ϵA�п�����Һ����ɫ�����к�ɫ�������ɣ���д�����ɺ�ɫ���ʵ����ӷ���ʽ ��
����ʹA�е����ܽ⣬�������м�����Լ������ ����ѡ����ĸ���ţ�
A��������HNO3 B��������NaOH C��������H2O2
�÷�Ӧ�����ӷ���ʽΪ ��
��ȡ5��00 g������Ʒ�������¶�ʹ��ֽ⣬�ֽ���̵��������ߣ���Ʒ�������¶ȱ仯�����ߣ�����ͼ��ʾ��

����ͼ�п��Կ����������ֽ������¶��� ��
��ͨ������ȷ��258��ʱ������Ӧ�Ļ�ѧ����ʽΪ ��e���Ӧ�Ļ�ѧʽΪ �����������ȥ����

��������Cu2Sұ��ͭ����ȡCuSO4��5H2O������ͼ��

��Cu2S��ͭԪ�صĻ��ϼ�Ϊ ������1molCu2S��O2��Ӧ����2molCuʱ��ת�Ƶ��ӵ����ʵ����� ��
��Cu2O��CuO�м�������ϡ����õ�����ϵA�п�����Һ����ɫ�����к�ɫ�������ɣ���д�����ɺ�ɫ���ʵ����ӷ���ʽ ��
����ʹA�е����ܽ⣬�������м�����Լ������ ����ѡ����ĸ���ţ�
A��������HNO3 B��������NaOH C��������H2O2
�÷�Ӧ�����ӷ���ʽΪ ��
��ȡ5��00 g������Ʒ�������¶�ʹ��ֽ⣬�ֽ���̵��������ߣ���Ʒ�������¶ȱ仯�����ߣ�����ͼ��ʾ��

����ͼ�п��Կ����������ֽ������¶��� ��
��ͨ������ȷ��258��ʱ������Ӧ�Ļ�ѧ����ʽΪ ��e���Ӧ�Ļ�ѧʽΪ �����������ȥ����
��1��+1 �� 6mol ��2��Cu2O + 2H+ =" Cu" + Cu2+ +H2O ��3��C�� Cu + H2O2 + 2H+ =Cu2+ +H2O
��4��102�� �� CuSO4��H2O CuSO4 + H2O �� Cu2O
CuSO4 + H2O �� Cu2O
��4��102�� �� CuSO4��H2O
 CuSO4 + H2O �� Cu2O
CuSO4 + H2O �� Cu2O�����������1��Cu2S��Cu2Oһ����ͭ�Ļ��ϼ۶���+1�ۣ����Զ������շ�Ӧ����ɵ���ͭ�����ϼ۽��ͣ�����2molͭ��ת�Ƶ���2mol��
��2��Cu2O�м�������ϡ��������ΪCu2O�������绯��Ӧ��0�ۡ� +1 ��+2�ۣ������к�ɫ�������ɡ�Cu2O + 2H+ =" Cu" + Cu2+ +H2O
��3��Ҫʹ����ͭ�������ͭ��Ӧ�ü�����������ͭ�������������Dz��������ʺͻ�����Ӧ��ѡ��C�� H2O2 �����������¿���Cu����ΪCu2+ ������ʽΪ��Cu + H2O2 + 2H+ =Cu2+ +H2O��
��4������ͼ���֪�����¶ȵ����ߣ�������Ʒ�����������١���102��ʱ��һ�γ����������٣����Ե�����ʼ���ַֽ⣬���¶ȴﵽ258��ʱ��5g��Ʒ������1��8g�����Ը��ݱ�����֪��ʱ�����еĽᾧˮǡ��ȫ��ʧȥ�����Է�ӦΪ��CuSO4��H2O
 CuSO4 + H2O�����¶ȴﵽ1000��ʱ������e�������Ѿ����ټ��٣����Դ�ʱCuSO4 �����ֽ�����Cu2O��
CuSO4 + H2O�����¶ȴﵽ1000��ʱ������e�������Ѿ����ټ��٣����Դ�ʱCuSO4 �����ֽ�����Cu2O��
��ϰ��ϵ�д�
 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
�����Ŀ